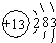��Ŀ����
��ͼ��Ԫ�����ڱ��Ŀ�ܣ����ڱ��Т١���Ԫ���лش�����
|
�� |
|
|
|||||||||||||||
|
|
|
|
|
|
�� |
�� |
�� |
|
|||||||||
|
�� |
�� |
�� |
|
|
|
�� |
|
||||||||||
|
�� |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
�� |
|
���û�ѧ���Իش��������⣺
��1���ڱ��Тܡ��ݡ�������Ԫ�صļ����Ӱ뾶�ɴ�С��˳��Ϊ__________________________��
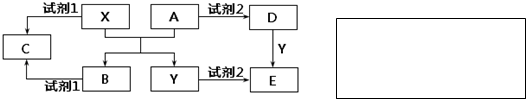
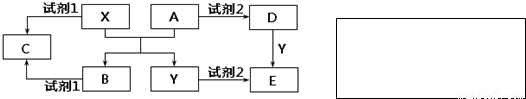
(2)���Т������Ԫ�ص�����������ˮ���ﷴӦ�����ӷ���ʽΪ_______________________��
(3)���������Ԫ�طǽ�����ǿ����________������һ�����ӷ���ʽ֤���ý���_________��
(4)����۵����ֵ��ʿ����ڽ��������缫ʱ����һ�ֶԻ����Ѻõ�ȼ�ϵ�أ������Ϊ�������������ˮ�������д��������Ӧʽ_____________________����ع���ʱ�����Ӷ����ƶ���________������������
(5)Ԫ�آ��������ֵ�����һ�������¿ɷ�Ӧ����һ�ֻ�����ף���֪�±��е��������ƻ�1 mol�����еĻ�ѧ�������յ�������kJ����������1mol��ʱ�ͷŵ�����Ϊ____________kJ��
|
��ѧ�� |
Cl2 |
Br2 |
I2 |
HCl |
HBr |
HI |
H2 |
|
������kJ�� |
243 |
193 |
151 |
432 |
366 |
298 |
436 |
��1�� F->Na+>Mg2+ ����2�� Al��OH��3+OH-=AlO2-+2H2O ��
��3�� Cl>Br Cl2+2Br-=2Cl-+Br2 ��
��4�� O2+4e- +2H2O=4OH�� �� �� ������5�� 92.5 kJ��
��������
�������������ͼ�����ƶϳ��١��ڡ��ۡ��ܡ��ݡ��ޡ��ߡ��ࡢ�ᡢ��ֱ�ΪH��N��O��F��Na��Mg��Al��Cl��K��Br����1���У��ܡ��ݡ��ֱ�ΪF��Na��Mg���������Ӱ뾶�ɴ�С��˳��ΪF->Na+>Mg2+��(2)�������Ԫ�ص�����������ˮ����ֱ�Ϊ�������ƺ������������������ߵķ�Ӧ�����ӷ���ʽΪAl��OH��3+OH-=AlO2-+2H2O��(3)���������Ԫ�طǽ�����ǿ����Cl>Br,����ͨ�����廯����Һ��ͨ�����������飬���������ӷ���ʽΪCl2+2Br-=2Cl-+Br2��(4) )����۵����ֵ����ڽ��������缫ʱ����һ�ֶԻ����Ѻõ�ȼ�ϵ��Ϊ����ȼ�ϵ�أ�������������Ϊ�������Һ��������������ӦʽΪO2+4e- +2H2O=4OH�������ڸ��������������ӣ����Ե�ع���ʱ�����Ӷ����ƶ���������(5)Ԫ�آ��������ֵ�����һ�����������ɵĻ�����ΪHCl���仯ѧ��Ӧ����ʽΪ��H2��Cl2=2HCl������1mol��ʱ�ͷŵ�����Ϊ( 432-436-243)/2="92.5" Kj.
432-436-243)/2="92.5" Kj.
���㣺Ԫ�����ڱ�
���������⿼����Ԫ�����ڱ��в���Ԫ�ؼ��仯��������ʣ�������Ϣ���Ƚϴ���һ�����ۺ��ԣ���һ���������ƶ��⡣

 ��ǰ����ϵ�д�
��ǰ����ϵ�д�