题目内容
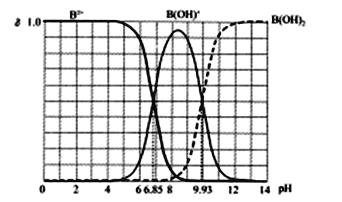
【题目】25℃某二元碱B(OH)2水溶液中,B2+、B(OH)+和B(OH)2三者各自的物质的量分数δ随溶液pH的变化曲线如图所示,下列说法错误的是(已知多元碱的电离是逐级进行的)
A. Kb2[B(OH)2]的数量级为10-8
B. 在B(OH)Cl溶液中c(OH-)>c(H+)
C. 等物质的量的BCl2和B(OH)Cl混合溶液中δ(B2+)<δ[B(OH)+]
D. B(OH)Cl溶液中,若c[B(OH)2]+2c(B2+)+c(H+)-c(OH-),则δ[B(OH)2]=δ[B(OH)+]
【答案】D
【解析】根据图像可知,当c(H+)=10-6 mol/L时,c(OH-)= 10-8 mol/L, c(B2+)= (B(OH)+), 带入公式Kb2[B(OH)2]= c(B2+)×c(OH-)/ c(B(OH)+)=10-8 mol/L,A正确;在B(OH)Cl溶液,完全电离出B2+、Cl-、OH-,溶液显碱性,c(OH-)>c(H+),B正确;BCl2溶液水解显酸性,加入碱性溶液B(OH)Cl,促进了BCl2的水解,导致B(OH)+的量增大,B2+的量减小,所以δ(B2+)<δ[B(OH)+],C正确;根据电荷守恒规律:c(OH-)+ c(Cl-)= c(H+)+ c(B(OH)+)+2c(B2+),然后把c[B(OH)2]+2c(B2+)+c(H+)=c(OH-)带入上式中,结果为:c(Cl-)+ c[B(OH)2]= c(B(OH)+),D错误;正确选项D。

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目