题目内容
(1)(浙江高考)对于气相反应,用某组分(B)的平衡压强(pB)代替物质的量浓度(cB)也可表示平衡常数(记作Kp),则反应CH4(g)+H2O(g) CO(g)+3H2(g) ΔH=206.2 kJ·mol-1的Kp=________,随着温度的升高,该平衡常数________(填“增大”“减小”或“不变”)。
CO(g)+3H2(g) ΔH=206.2 kJ·mol-1的Kp=________,随着温度的升高,该平衡常数________(填“增大”“减小”或“不变”)。
(2)(天津高考)写出WO3(s)+3H2(g) W(s)+3H2O(g)的化学平衡常数表达式为________。
W(s)+3H2O(g)的化学平衡常数表达式为________。
(3)(福建高考)在恒容绝热(不与外界交换能量)条件下进行2A(g)+B(g)??2C(g)+D(s)反应,按下表数据投料,反应达到平衡状态,测得体系压强升高。简述该反应的平衡常数与温度的变化关系:________。
 CO(g)+3H2(g) ΔH=206.2 kJ·mol-1的Kp=________,随着温度的升高,该平衡常数________(填“增大”“减小”或“不变”)。
CO(g)+3H2(g) ΔH=206.2 kJ·mol-1的Kp=________,随着温度的升高,该平衡常数________(填“增大”“减小”或“不变”)。(2)(天津高考)写出WO3(s)+3H2(g)
 W(s)+3H2O(g)的化学平衡常数表达式为________。
W(s)+3H2O(g)的化学平衡常数表达式为________。(3)(福建高考)在恒容绝热(不与外界交换能量)条件下进行2A(g)+B(g)??2C(g)+D(s)反应,按下表数据投料,反应达到平衡状态,测得体系压强升高。简述该反应的平衡常数与温度的变化关系:________。
| 物质 | A | B | C | D |
| 起始投料/mol | 2 | 1 | 2 | 0 |
(1)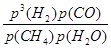 增大
增大
(2)K=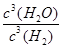
(3)平衡常数随温度升高而变小
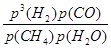 增大
增大(2)K=
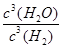
(3)平衡常数随温度升高而变小
(1)据题中Kp的描述可知,Kp=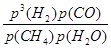 。该反应为吸热反应,温度升高,平衡正向移动,Kp增大。
。该反应为吸热反应,温度升高,平衡正向移动,Kp增大。
(2)根据反应的化学方程式可知,该反应的平衡常数表达式为K=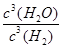 。(3)该反应的正反应是一个气体分子数减小的反应,反应达到平衡状态,体系压强升高,说明正反应是一个放热反应,升高温度,平衡向左移动,即化学平衡常数随温度升高而减小。
。(3)该反应的正反应是一个气体分子数减小的反应,反应达到平衡状态,体系压强升高,说明正反应是一个放热反应,升高温度,平衡向左移动,即化学平衡常数随温度升高而减小。
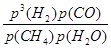 。该反应为吸热反应,温度升高,平衡正向移动,Kp增大。
。该反应为吸热反应,温度升高,平衡正向移动,Kp增大。(2)根据反应的化学方程式可知,该反应的平衡常数表达式为K=
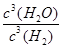 。(3)该反应的正反应是一个气体分子数减小的反应,反应达到平衡状态,体系压强升高,说明正反应是一个放热反应,升高温度,平衡向左移动,即化学平衡常数随温度升高而减小。
。(3)该反应的正反应是一个气体分子数减小的反应,反应达到平衡状态,体系压强升高,说明正反应是一个放热反应,升高温度,平衡向左移动,即化学平衡常数随温度升高而减小。
练习册系列答案
 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
 2Q(g)+nR(g),达到平衡后,容器内的压强比原来增加5%,X浓度减小
2Q(g)+nR(g),达到平衡后,容器内的压强比原来增加5%,X浓度减小 ,则该反应方程式中的n值是( )
,则该反应方程式中的n值是( ) C(g)+D(g),5 min后达平衡,已知各物质的平衡浓度的关系为ca(A)·c(B)=c(C)·c(D)。若在温度不变的情况下,将容器的体积扩大为原来的10倍,A 的转化率没有发生变化,则B的转化率为( )
C(g)+D(g),5 min后达平衡,已知各物质的平衡浓度的关系为ca(A)·c(B)=c(C)·c(D)。若在温度不变的情况下,将容器的体积扩大为原来的10倍,A 的转化率没有发生变化,则B的转化率为( ) CdS(s)+2H+(aq) ΔH<0
CdS(s)+2H+(aq) ΔH<0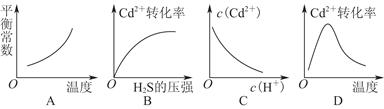
 Ni(CO)4(g),已知该反应在25 ℃和80 ℃时的平衡常数分别为5×104、2,下列说法正确的是( )。
Ni(CO)4(g),已知该反应在25 ℃和80 ℃时的平衡常数分别为5×104、2,下列说法正确的是( )。 ?2C(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中各物质的物质的量浓度、反应速率分别随时间的变化如下图所示:
?2C(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中各物质的物质的量浓度、反应速率分别随时间的变化如下图所示: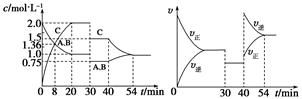
 2SO3(g) ΔH=-Q kJ/mol,测得SO2的转化率为90%,则在此条件下反应放出的热量为
2SO3(g) ΔH=-Q kJ/mol,测得SO2的转化率为90%,则在此条件下反应放出的热量为 2SO3(g) ΔH="-Q" kJ·mol-1。在上述条件下分别充入的气体和反应放出的热量(Q)如表所列:
2SO3(g) ΔH="-Q" kJ·mol-1。在上述条件下分别充入的气体和反应放出的热量(Q)如表所列: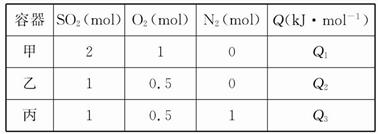
 N2O4(g) ,平衡后,向容器内再充入1molNO2,下列说法正确的
N2O4(g) ,平衡后,向容器内再充入1molNO2,下列说法正确的