题目内容
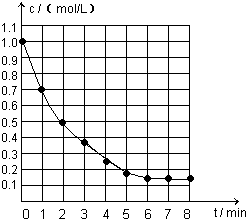 右图表示反应X(g)
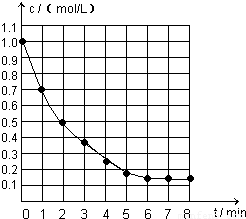
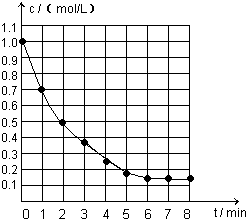
右图表示反应X(g) 4Y(g)+Z(g),△H<0,在某温度时X的浓度随时间变化的曲线:
4Y(g)+Z(g),△H<0,在某温度时X的浓度随时间变化的曲线:下列有关该反应的描述正确的是( )
分析:根据图可知,X的浓度在随时间逐渐减少,到第6min浓度不再变化,则反应达到化学平衡;利用X变化的量来计算转化率,再利用温度对反应的影响来分析转化率的变化及反应速率的变化.
解答:解:A、6min时反应达平衡,但未停止,故A错;
B、X的变化量为1mol/L-0.15mol/L=0.85mol/L,则X的转化率为
×100%=85%,故B正确;
C、△H<0,反应为放热,故升高温度,平衡将逆向移动,则X的转化率减小,故C错;
D、降温时,正、逆反应速率同时减小,但是降温平衡正向移动,故V正>V逆,即逆反应减小的倍数大,故D错误;
故选:B.
B、X的变化量为1mol/L-0.15mol/L=0.85mol/L,则X的转化率为
| 0.85mol/L |
| 1.0mol/L |
C、△H<0,反应为放热,故升高温度,平衡将逆向移动,则X的转化率减小,故C错;
D、降温时,正、逆反应速率同时减小,但是降温平衡正向移动,故V正>V逆,即逆反应减小的倍数大,故D错误;
故选:B.
点评:本题考查物质的浓度随时间的变化图象,明确纵横坐标的意义及影响化学平衡和化学反应速率的因素是解答的关键,尤其注意温度对反应速率及平衡移动的影响,不可混淆.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
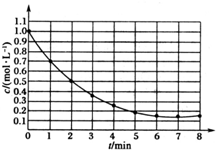 19、右图表示反应X(g)
19、右图表示反应X(g) 4Y(g)
+Z(g) △H < 0,在某温度时X的浓度随时间变化的曲线:
4Y(g)
+Z(g) △H < 0,在某温度时X的浓度随时间变化的曲线: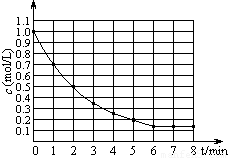

 4Y(g)+Z(g),△H<0,在某温度时X的浓度随时间变化的曲线:
4Y(g)+Z(g),△H<0,在某温度时X的浓度随时间变化的曲线: