题目内容
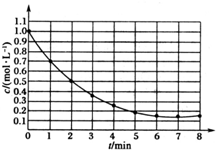 19、右图表示反应X(g)
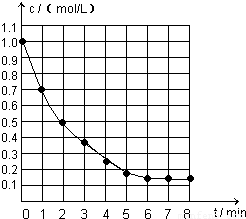
19、右图表示反应X(g)分析:根据图可知,X的浓度在随时间逐渐减少,到第6min浓度不再变化,则反应达到化学平衡;利用X变化的量来计算转化率,根据v=
计算X的平均反应速率.
| △C |
| △t |
解答:解:A、6min时反应达平衡,但未停止,故A错误;
B、X的变化量为1mol/L-0.15mol/L=0.85mol/L,则X的转化率为
×100%=85%,故B正确;
C、从反应开始到反应达到平衡状态的时间为6min,但6min后该反应未停止,仍在继续反应,只是正逆反应速率相等,是一个动态平衡状态,故C错误.
D、在1min内X的平均反应速率=
=0.3mol?L-1?min-1,故D错误.
故选B.
B、X的变化量为1mol/L-0.15mol/L=0.85mol/L,则X的转化率为
| 0.85mol/L |
| 1mol/L |
C、从反应开始到反应达到平衡状态的时间为6min,但6min后该反应未停止,仍在继续反应,只是正逆反应速率相等,是一个动态平衡状态,故C错误.
D、在1min内X的平均反应速率=
| (1.0-0.7)mol/L |
| 1min |
故选B.
点评:本题考查物质的浓度随时间的变化图象,明确纵横坐标的意义是解答本题的关键.

练习册系列答案
相关题目
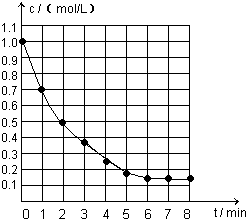 右图表示反应X(g)
右图表示反应X(g) 4Y(g)+Z(g),△H<0,在某温度时X的浓度随时间变化的曲线:
4Y(g)+Z(g),△H<0,在某温度时X的浓度随时间变化的曲线: 4Y(g)
+Z(g) △H < 0,在某温度时X的浓度随时间变化的曲线:
4Y(g)
+Z(g) △H < 0,在某温度时X的浓度随时间变化的曲线: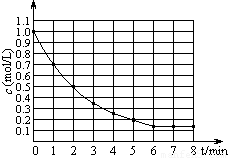

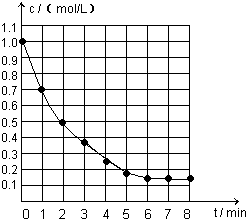
 4Y(g)+Z(g),△H<0,在某温度时X的浓度随时间变化的曲线:
4Y(g)+Z(g),△H<0,在某温度时X的浓度随时间变化的曲线: