题目内容
【题目】铁制品容易生锈,对钢铁制品防腐措施合理的是
A. 暂时不使用的铁锅涂上油 B. 铁质自来水管缠上铜线
C. 铜铁帽的防护栏涂上油漆 D. 自行车钢圈镀铬
【答案】ACD
【解析】根据铁在与水和氧气并存时易生锈,据此解答。
A. 暂时不使用的铁锅涂上油隔绝了铁与氧气、水的接触,起到了防锈的目的,A正确;
B. 铁质自来水管缠上铜线形成原电池,铁是负极失去电子被腐蚀,B错误;
C. 铜铁帽的防护栏涂上油漆隔绝了铁与氧气、水的接触,起到了防锈的目的,C正确;
D. 自行车钢圈镀铬可起到防锈的目的,D正确。答案选ACD。

【题目】(题文)为探究Ag+与Fe3+氧化性的相关问题,某小组同学进行如下实验:
已知:相关物质的溶解度(20℃) Ag2SO4:0.796 g
(1)甲同学的实验如表:
序号 | 操作 | 现象 |
实验Ⅰ | 将2mL 1 molL-1 AgNO3溶液加入到1mL 1 molL-1 FeSO4溶液中 | 产生白色沉淀,随后又有黑色固体产生 |
取上层清液,滴加KSCN溶液 | 溶液变红 |
注:经检验黑色固体为Ag。
①白色沉淀的化学式是__________________。
②甲同学得出Ag+氧化了Fe2+的依据是_____________________________________。
(2)乙同学为探究Ag+和Fe2+的反应,进行实验II。
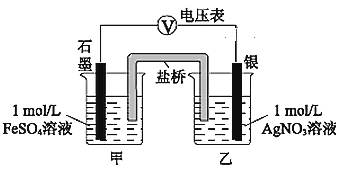
a.按如图连接装置并加入药品(盐桥中的物质不参与反应),发现电压表指针偏移。偏移的方向表明:电子由石墨经导线流向银。放置一段时间后,指针偏移减小。
①盐桥中盛有饱和KNO3溶液,此盐桥中钾离子向________(填“甲”或“乙”)池移动;
②若该电池能维持稳定电流强度为1 A,工作600s,理论上Ag电极的质量会________(填“增重”或“溶解”) ________g(已知F=96500 C·mol-1,电量(C)=电流(A)×时间(s) )。
b.随后向甲烧杯中逐渐加入浓Fe2(SO4)3溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
③a中甲烧杯里的电极反应式是______________。
④b中电压表指针逆向偏移后,银为_______(填“正”或“负”)极。
(3)由上述实验得出的结论为_________________________________________________。
【题目】乙醇是重要的化工原料和液体燃料,可以利用下列反应制取乙醇:2CO2(g) + 6H2(g) ![]() CH3CH2OH(g) + 3H2O(g)
CH3CH2OH(g) + 3H2O(g)
(1)写出该反应的平衡常数表达式:K=_________________________。
(2)请说明以CO2为原料合成乙醇的优点是_____________________(只要求写出一条)。
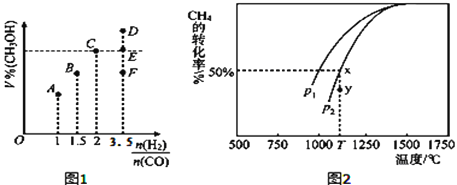
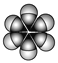
(3)在一定压强下,测得该反应的实验数据如下表:
| 500 | 600 | 700 | 800 |
1.5 | 45 | 33 | 20 | 12 |
2.0 | 60 | 43 | 28 | 15 |
3.0 | 83 | 62 | 37 | 22 |
① 该反应是___________反应(填“吸热”或“放热”)。
② 一定条件下,若提高氢碳比[n(H2)/n(CO2)],则CO2的转化率______________(填“增大”、“减小”、或“不变”)
(4)一种乙醇燃料电池中发生的化学反应为:在酸性溶液中乙醇与氧作用生成水和二氧
化碳。该电池的负极反应式为:_______________________________________。
(5)25℃、101 kPa下,H2(g)、C2H4(g)和C2H5OH(l)的燃烧热分别是285.8 kJ · mol-1、1411.0 kJ · mol-1和1366.8 kJ · mol-1,请写出由C2H4(g)和H2O(l)反应生成C2H5OH(l)的热化学方程式____________________________________________________。
【题目】观察下列比例模型,每个模型表示的分子均由C、H、O中的两种或三种构成。对各模型表示的物质的相关叙述正确的是( )
比例模型 | 对模型表示的物质的相关叙述 | |
A |
| 将形状、大小均相同的金属钠分别投入盛有0.1 mol/L的该物质的水溶液、无水乙醇和水的烧杯中,盛该物质的烧杯中产生气泡的速率最慢 |
B |
| 将灼热的铜丝反复插入盛有该物质的试管中,观察到铜丝由黑色变为光亮的红色并产生有刺激性气味的物质。此反应体现了该物质的氧化性 |
C |
| 在分液漏斗中加入该物质与碘水的混合液,充分振荡,碘水褪色,此时发生了取代反应 |
D |
| 该物质及其碳原子数小于10的同系物中,一氯代物只有一种(不考虑立体异构)的物质共有4种 |
A. A B. B C. C D. D