题目内容
【题目】CO、H2是煤的气化产物,在生产生活中用途广泛。
(1)CO还原法处理大气污染物SO2
①2CO(g) + SO2(g) ![]() S(s)+2CO2(g) H = -270 kJ·mol-1,该反应的平衡常数表达式为__。
S(s)+2CO2(g) H = -270 kJ·mol-1,该反应的平衡常数表达式为__。
②在绝热恒容的密闭容器中进行上述反应,下列说法正确的是_____。
a 若混合气体密度保持不变,则已达平衡状态
b 达平衡后若再充人一定量CO2,平衡常数保持不变
c 分离出部分S,正、逆反应速率均保持不变,平衡不移动
d 从反应开始到平衡,容器内气体的压强保持不变
③向2 L恒温恒容密闭容器中通人2 mol CO、1 mol SO2,分别进行a、b、c三组实验。在不同催化剂件下发生反应:2CO(g) + SO2(g) ![]() S(s)+2CO2(g) H = -270 kJ·mol-1,反应体系总压随时间的变化如下表所示,则三组实验温度的大小关系是_____(用a、b、c表示),实验a从反应开始至45s达到平衡,则该过程反应速率v(SO2)__________(结果保留2位有效数字)。
S(s)+2CO2(g) H = -270 kJ·mol-1,反应体系总压随时间的变化如下表所示,则三组实验温度的大小关系是_____(用a、b、c表示),实验a从反应开始至45s达到平衡,则该过程反应速率v(SO2)__________(结果保留2位有效数字)。
| 0s | 40s | 45s | 60s |
a | 175 | 142 | 140 | 140 |
b | 160 | 120 | 120 | 120 |
c | 160 | 130 | 125 | 120 |
(2)利用CO、H2可制备天然气,主要反应为:
CO(g) + 3H2(g) ![]() CH4(g) + H2O(g) H1=-206.2 kJ·mol-1;
CH4(g) + H2O(g) H1=-206.2 kJ·mol-1;
CO(g) + H2O(g) ![]() CO2(g) + H2(g) H2 = -41.0 kJ·mol-1;
CO2(g) + H2(g) H2 = -41.0 kJ·mol-1;
H2O(l) ═H2O(g) H3 =+44 kJ·mol-1 。
回答下列问题:
①反应CO2(g) + 4H2(g) ![]() CH4(g) + 2H2O(l) 的H4 = ________ kJ·mol-1。某温度下,分别在起始容积相同的恒压容器A、恒容容器B中加人1molCO2和4molH2的混合气体,两容器反应达到平衡后放出或吸收的热量较多的是__( 填“A”或“B")。
CH4(g) + 2H2O(l) 的H4 = ________ kJ·mol-1。某温度下,分别在起始容积相同的恒压容器A、恒容容器B中加人1molCO2和4molH2的混合气体,两容器反应达到平衡后放出或吸收的热量较多的是__( 填“A”或“B")。
②在恒压管道反应器中按n(H2):n(CO) = 3:1通入原料气,在催化剂作用下制备合成天然气,400 ℃ p总为100 kPa时反应体系平衡组成如下表所示:
组分 | CH4 | H2O | H2 | CO2 | CO |
体积分数/% | 45.0 | 42.5 | 10.0 | 1.50 | 1.00 |
则该条件下CO的总转化率α=____。![]()
③制备合成天然气采用在原料气中通入水蒸气来缓解催化剂积碳。
积碳反应为:反应I :CH4(g) ![]() C(s) + 2H2(g) H = +75 kJ·mol-1;
C(s) + 2H2(g) H = +75 kJ·mol-1;
反应Ⅱ:2CO(g) ![]() C(s) + CO2(g) H = -172 kJ·mol-1,
C(s) + CO2(g) H = -172 kJ·mol-1,
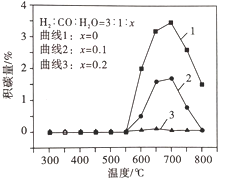
平衡体系中水蒸气浓度对积碳量的影响如图所示,下列说法正确的是__。
A 曲线1在700 ~ 800℃积碳量减小的原因可能是反应Ⅱ逆向移动
B 曲线1在550 ~700℃积碳量增大的原因可能是反应I、Ⅱ的速率增大
C 曲线2、3在550 ~800℃积碳量较低的原因是水蒸气稀释作用使积碳反应速率减小
D 水蒸气能吸收反应放出的热量,降低体系温度至550℃以下,有利于减少积碳
【答案】![]() a c a>b=c 0.0067 mol/(L·s) -253.2 A 97.9% AD
a c a>b=c 0.0067 mol/(L·s) -253.2 A 97.9% AD
【解析】
(1) ①平衡常数直接根据表达式得出答案;②气相为主的反应中,固相物质的浓度项不列入反应的平衡常数表达式,结合常用判断化学平衡的方法判断化学反应是否达到平衡,据此逐项分析;③理想气体状态方程PV=nRT,结合表格数据,可以比较出温度大小;计算反应速率,要计算出过程中SO2的消耗量即可。
(2) ①①CO(g) + 3H2(g) ![]() CH4(g) + H2O(g) H1=-206.2 kJ·mol-1;
CH4(g) + H2O(g) H1=-206.2 kJ·mol-1;
②CO(g) + H2O(g) ![]() CO2(g) + H2(g) H2 = -41.0 kJ·mol-1;
CO2(g) + H2(g) H2 = -41.0 kJ·mol-1;
③H2O(l) ═H2O(g) H3 =+44 kJ·mol-1 。
将方程式①-②-2x③得CO2(g) + 4H2(g) ![]() CH4(g) + 2H2O(l),△H进行相应的改变;A为恒温恒压、B为恒温恒容条件,如果是恒温恒容,反应前后物质的量减小、压强减小,开始时AB压强相等,B中压强逐渐减小A中压强不变,所以反应过程中压强A>B,增大压强平衡正向移动。
CH4(g) + 2H2O(l),△H进行相应的改变;A为恒温恒压、B为恒温恒容条件,如果是恒温恒容,反应前后物质的量减小、压强减小,开始时AB压强相等,B中压强逐渐减小A中压强不变,所以反应过程中压强A>B,增大压强平衡正向移动。
②设n(H2)=3mol、n(CO)=1mol,恒容恒温条件下气体的体积分数之比等于物质的量分数之比,设平衡时混合气体总物质的量为x mol,根据C原子守恒得![]() ,得x=2.11,则CO的转化率=
,得x=2.11,则CO的转化率=![]() ,该反应的正反应是放热反应,升高温度平衡逆向移动;
,该反应的正反应是放热反应,升高温度平衡逆向移动;
③A.反应II的逆反应是消碳反应;B.反应I、II的正反应都是积碳反应;C.高温条件下水蒸气和C反应生成CO和氢气;D.温度至550℃以下,几乎没有积碳。
(1) ①平衡常数表达式![]() ,故答案为:
,故答案为:![]() ;
;
②绝热恒容的密闭容器进行可以反应,
a. 混合气体密度为ρ=m/v,恒容容器容积V不变,反应前后气体的质量发生改变,则当反应到达平衡时,气体总质量m不变,因此若混合气体密度保持不变可以说明反应已经达到平衡状态,可知a正确;
b. 充人一定量CO2,反应移向移动,吸热,容器绝热,温度降低,平衡常数保持变化,b错误;
c.固体不影响平衡反应进行,故都不变,c正确;
d. 反应达到平衡前后,气体总物质的量发生改变,则体系压强改变,d错误;
ac正确,故答案为:a c;
③体系c和体系b反应起始时和平衡时的压强都相等,则二者平衡常数相同,体系c和体系b的温度相等,根据理想气体状态方程![]() ,初始时刻压强a>b,则实验温度a>b,因此三组实验温度的关系是a>b=c,故答案为:a>b=c;
,初始时刻压强a>b,则实验温度a>b,因此三组实验温度的关系是a>b=c,故答案为:a>b=c;
实验a从反应开始至平衡时,压强由175kPa改变至140kPa,设反应过程转化了xmol SO2,由理想气体状态方程可知,压强与气体总物质的量成正比,所以有![]() ,解得x=0.6mol,则反应速率
,解得x=0.6mol,则反应速率![]() ,故答案为:0.0067 mol/(L·s);
,故答案为:0.0067 mol/(L·s);
(2) ①①CO(g) + 3H2(g) ![]() CH4(g + H2O(g) H1=-206.2 kJ·mol-1;
CH4(g + H2O(g) H1=-206.2 kJ·mol-1;
②CO(g) + H2O(g) ![]() CO2(g) + H2(g) H2 = -41.0 kJ·mol-1;
CO2(g) + H2(g) H2 = -41.0 kJ·mol-1;
③H2O(l) ═H2O(g) H3 =+44 kJ·mol-1 。
将方程式①-②-2x③得CO2(g) + 4H2(g) ![]() CH4(g) + 2H2O(l),△H=-253.2 kJ·mol-1,;A为恒温恒压、B为恒温恒容条件,如果是恒温恒容,反应前后物质的量减小、压强减小,开始时AB压强相等,B中压强逐渐减小A中压强不变,所以反应过程中压强A>B,增大压强平衡正向移动,故答案为:-253.2;A;
CH4(g) + 2H2O(l),△H=-253.2 kJ·mol-1,;A为恒温恒压、B为恒温恒容条件,如果是恒温恒容,反应前后物质的量减小、压强减小,开始时AB压强相等,B中压强逐渐减小A中压强不变,所以反应过程中压强A>B,增大压强平衡正向移动,故答案为:-253.2;A;
②设n(H2)=3mol、n(CO)=1mol,恒容恒温条件下气体的体积分数之比等于物质的量分数之比,设平衡时混合气体总物质的量为x mol,根据C原子守恒得![]() ,得x=2.11,则CO的转化率=
,得x=2.11,则CO的转化率=![]() ,该反应的正反应是放热反应,升高温度平衡逆向移动;
,该反应的正反应是放热反应,升高温度平衡逆向移动;
③A.反应II的逆反应是消碳反应,曲线1在700-800℃积碳量减小的原因可能是反应Ⅱ逆向移动,且反应II的消碳量大于反应I的积碳量,故A正确;
B.反应I、II的正反应都是积碳反应,曲线1在550-700℃时两个反应没有达到平衡状态,都向正反应方向移动,导致积碳量增加,故B错误;
C.高温条件下水蒸气和C反应生成CO和氢气,从而使积碳量减少,故C错误;
D.温度至550℃以下,几乎没有积碳,所以水蒸气能吸收反应放出的热量,降低体系温度至550℃以下,有利于减少积碳,故D正确;
故选AD。

 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案