题目内容
6.根据下列物质中硫的化合价判断,下列说法错误的是( )| A. | Na2S具有还原性 | B. | SO2既有氧化性又有还原性 | ||
| C. | 浓H2SO4 具有氧化性 | D. | SO3 具有还原性 |
分析 由元素的化合价可知,处于最高价的元素的微粒具有氧化性,处于最低价的元素的微粒具有还原性,而处于中间价态的微粒既有氧化性又有还原性,以此来解答.
解答 解:A.Na2S中S元素的化合价为-2价,为最低价,则Na2S具有还原性,故A正确;
B.SO2中S元素的化合价为+4价,为中间价态,则SO2既有氧化性又有还原性,故B正确;
C.浓H2SO4中S元素的化合价为+6价,为最高价,则浓H2SO4具有氧化性,故C正确;
D.SO3中S元素的化合价为+6价,为最高价,则SO3具有氧化性,故D错误;
故选D.
点评 本题考查物质的性质,熟悉S元素的常见化合价及化合价与物质的性质的关系是解答本题的关键,题目难度不大.

练习册系列答案
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
16.下列叙述正确的是( )
| A. | 1molH2O的质量是18g/mol | |
| B. | CH4的摩尔质量是16g | |
| C. | 3.01×1023个CO2分子的质量是22g | |
| D. | 标准状况下,1mol任何物质的体积均为22.4L |
17.已知分解1molH2O2放出热量98kJ.在含有少量I-的溶液中,H2O2分解的机理为:
H2O2+I-→H2O+IO-
H2O2+IO-→H2O+O2+I-.
下列有关该反应的说法不正确的是( )
H2O2+I-→H2O+IO-
H2O2+IO-→H2O+O2+I-.
下列有关该反应的说法不正确的是( )
| A. | H2O2(l)═2H2O(g)+O2(g)△H=-196kJ•mol-1 | |
| B. | 在该反应中H2O2既做氧化剂.又做还原剂 | |
| C. | 反应速率与I-浓度有关 | |
| D. | v(H2O2)=v(H2O)=v(O2) |
14.化学与生活密切相关,下列说法不正确的是( )
| A. | 乙烯可作水果的催熟剂 | B. | 硅胶可作袋装食品的干燥剂 | ||
| C. | 二氧化硫可作食品的漂白剂 | D. | 氢氧化铝可作胃酸的中和剂 |
11.下列说法正确的是( )
| A. | 可食用植物油含有的高级脂肪酸甘油酯是人体的营养物质 | |
| B. | 石油的分馏、煤的液化和气化都是物理变化,石油的裂化、裂解都是化学变化 | |
| C. | 淀粉、蛋白质、葡萄糖都是高分子化合物 | |
| D. | 以重油为原料裂解得到各种轻质油 |
18.将蓝色石蕊试纸浸入氯水中后再取出,观察到的现象是( )
| A. | 蓝色不变 | B. | 试纸呈红色 | ||
| C. | 试纸先变红,再变白 | D. | 试纸立即变白 |
15.下列说法中,正确的是( )
| A. | 22.4 L N2含阿伏加德罗常数个氮分子 | |
| B. | 在标准状况下,22.4 L水的质量约为18 g | |
| C. | 22 g二氧化碳与标准状况下11.2 L HCl含有相同的分子数 | |
| D. | 标准状况下,相同体积的任何气体单质所含的原子数相同 |
16.下列关于卤族元素的比较中,错误的是( )
| A. | 气态氢化物稳定性:HF>HCl>HBr>HI | B. | 单质氧化性:F2>Cl2>Br2>I2 | ||
| C. | 元素的非金属性:F>Cl>Br>I | D. | 离子的还原性:F->Cl->Br->I- |
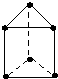 新合成的一种烃,其碳架呈三棱柱体(如图所示),小黑点表示碳原子,氢原子未标出.
新合成的一种烃,其碳架呈三棱柱体(如图所示),小黑点表示碳原子,氢原子未标出. .
.