题目内容
【题目】Bodensteins研究反应H2(g)+I2(g)![]() 2HI(g) △H<0 ,温度为T时,在两个体积均为1L的密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数w(HI)与反应时间t的关系如下表:
2HI(g) △H<0 ,温度为T时,在两个体积均为1L的密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数w(HI)与反应时间t的关系如下表:
容器编号 | 起始物质 | t/min | 0 | 20 | 40 | 60 | 80 | 100 |
Ⅰ | 0.5molI2、0.5molH2 | w(HI)/% | 0 | 50 | 68 | 76 | 80 | 80 |
Ⅱ | xmolHI | w(HI)/% | 100 | 91 | 84 | 81 | 80 | 80 |
研究发现上述反应中:v正=kaw(H2)w(I2),v逆=kbw2(HI),其中ka、kb为常数。下列说法不正确的是( )
A. 温度为T时,该反应![]() =64
=64
B. 容器I中在前20min的平均速率v(HI)=0.025molL-1min-1
C. 若起始时,向容器I中加入物质的量均为0.1mol的H2、I2、HI,反应逆向进行
. 无论x为何值,两容器中达平衡时w(HI)%均相同
【答案】C
【解析】
A. H2(g)+I2(g)2HI(g)
起始量(mol/L) 0.5 0.5 0
变化量(mol/L) n n 2n
平衡量(mol/L) 0.5-n 0.5-n 2n
w(HI)/%=![]() ×100%=80%,n=0.4 mol/L,平衡常数 K=
×100%=80%,n=0.4 mol/L,平衡常数 K=![]() =64。反应达到平衡状态时正逆反应速率相等,kaw(H2)w(I2)=v正=v逆=kbw2(HI),则
=64。反应达到平衡状态时正逆反应速率相等,kaw(H2)w(I2)=v正=v逆=kbw2(HI),则![]() =
=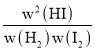 =K=64,故A正确;
=K=64,故A正确;
B.前20 min,H2(g) + I2(g)2HI(g)
起始量(mol/L) 0.5 0.5 0
变化量(mol/L) m m 2m
平衡量(mol/L) 0.5-m 0.5-m 2m
w(HI)%=![]() ×100%=50%,m=0.25mol/L,容器I中前20 min的平均速率,v(HI)=
×100%=50%,m=0.25mol/L,容器I中前20 min的平均速率,v(HI)=![]() =0.025molL-1min-1,故B正确;
=0.025molL-1min-1,故B正确;
C.若起始时,向容器I中加入物质的量均为0.l mol的H2、I2、HI,此时浓度商Qc=![]() =1<K=64,反应正向进行,故C错误;
=1<K=64,反应正向进行,故C错误;
D.H2(g)+I2(g)2HI(g)反应前后气体的物质的量不变,改变压强,平衡不移动,因此无论x为何值,Ⅰ和Ⅱ均等效,两容器达平衡时w(HI)%均相同,故D正确;
答案选C。