��Ŀ����
��һ�������£���������������������·�Ӧ��2SO2��g��+O2��g��?2SO3��g������H��0��
��1��д���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽK=
��2�������¶ȣ��÷�ӦKֵ ����������ת���� ����ѧ��Ӧ���� �����Ͼ�������С�䣩��
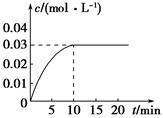
��3��600��ʱ����һ�ܱ������У������������������ϣ���Ӧ������SO2��O2��SO3���ʵ����仯��ͼ����Ӧ����ƽ��״̬��ʱ���� ��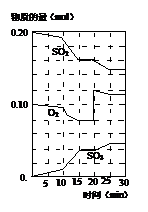
��4����ͼ�жϣ���Ӧ������20minʱ�����߷����仯��ԭ���� �������ֱ����
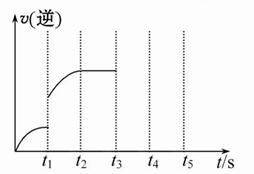
��5��10min��15min�����߱仯��ԭ������� ����д��ţ���
a�����˴��� b����С�������
c�������¶� d������SO3�����ʵ�����
��6����˵���÷�Ӧ�Ѿ��ﵽƽ��״̬���ǣ� ��
a�� v��SO3����2v��O2�� b��������ѹǿ���ֲ���
c��v�棨SO2��=2v����O2�� d���������������ʵ��ܶȱ��ֲ���
��7��Ϊʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ����ǣ� ��
a����ʱ�����SO3���� b���ʵ������¶�
c������O2��Ũ�� d��ѡ���Ч�Ĵ���
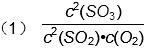
��2����������С
��3��15-20min��25-30min
��4��������������Ũ�Ȼ�����0.04mol����
��5��ab��6��bc��7��c
������2���÷�Ӧ����ӦΪ���ȷ�Ӧ�������¶�ƽ��������Ӧ�����ƶ���ƽ�ⳣ��k����������ת�����������¶ȷ�Ӧ���ʼ�С��
�ʴ�Ϊ����������С��
��3����Ӧ���������ʵ����ʵ������仯��˵����Ӧ����ƽ��״̬����ͼ��֪��15-20min��25-30min����ƽ̨������ֵ����ʵ������䣬��Ӧ����ƽ��״̬��
�ʴ�Ϊ��15-20min��25-30min��
��4����ͼ��֪����Ӧ������20minʱ��ƽ��������Ӧ�ƶ���˲��ֻ��������Ũ������Ӧ��������������Ũ�ȡ��ʴ�Ϊ��������������Ũ�ȡ�
��5����ͼ��֪����Ӧ������Ӧ���У�10min��15min��Ӧ����ﵥλʱ���ڵı仯������˵����Ӧ��������10min�ı�˲�䣬�����ʵ����ʵ������䡣
a�����˴���������Ӧ���ʣ���a��ȷ��
b����С�������������ѹǿ������Ӧ���ʣ���b��ȷ��
c�������¶ȷ�Ӧ���ʽ��ͣ���c����
d��10min�ı�˲�䣬�����ʵ����ʵ������䣬��������SO3�����ʵ�������d����
��ѡ��ab
��6��bc��7��c
���㣺����ƽ�ⳣ����ƽ���ƶ���ƽ��Ӱ��Ԫ�ء���ѧƽ��ͼ��ȣ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д���2 L�ܱ�������,800 ��ʱ��Ӧ2NO(g)+O2(g) 2NO2(g)��ϵ��,n(NO)��ʱ��ı仯���±�:
2NO2(g)��ϵ��,n(NO)��ʱ��ı仯���±�:
| ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |

(1)��ͼ��ʾNO2��Ũ�ȱ仯��������������������O2��ʾ��0~2 s�ڸ÷�Ӧ��ƽ������v=����������
(2)��˵���÷�Ӧ�Ѵﵽƽ��״̬��������������
a.v(NO2)=2v(O2) ����b.������ѹǿ���ֲ���
c.v��(NO)=2v��(O2) ����d.�������ܶȱ��ֲ���
ijͬѧΪ��̽��п�����ᷴӦ�����е����ʱ仯,����100 mLϡ�����м���������п��,����ˮ�������ռ���Ӧ�ų�������(�������������Ϊ��״��),ʵ���¼����(�ۼ�ֵ):
| ʱ��/min | 1 | 2 | 3 | 4 | 5 |
| �������/mL | 50 | 120 | 232 | 290 | 310 |
(1)��һʱ���(ָ0~1��1~2��2~3����4~5 min)��Ӧ���������_______,ԭ������_________________________��
(2)��һʱ��εķ�Ӧ������С��������,ԭ������_________________________
(3)��2~3 minʱ����������Ũ�ȱ仯����ʾ�ĸ÷�Ӧ������________________
(4)�����Ӧ̫����,Ϊ�˼�����Ӧ���ʶ��ֲ����ٲ�����������,���������зֱ����������������Һ:
A.����ˮ B.NaCl��Һ C.Na2CO3��Һ D.CuSO4��Һ
����Ϊ���е���(����)����������
�ϳɰ����������Ĵ����������˹��̵���;�����Ի�ѧ��ҵ����Ҳ�������ش�Ӱ�졣�ϳɰ���Ӧ�Ļ�ѧ����ʽΪN2(g)��3H2(g) 2NH3(g)����H����92.2 kJ��mol��1���ϳɰ���ҵ��ԭ����N2�ɴӿ����з���õ���H2���ü����̿��ˮ������Ӧ�Ƶá�
2NH3(g)����H����92.2 kJ��mol��1���ϳɰ���ҵ��ԭ����N2�ɴӿ����з���õ���H2���ü����̿��ˮ������Ӧ�Ƶá�
(1)��һ�ݻ��̶����ܱ�������ע��N2��H2�������壬����������Ӧ����ij�¶��´ﵽƽ��ʱ�������ʵ�Ũ�ȷֱ��ǣ�c(H2)��9.00 mol��L��1��c(N2)��3.00 mol��L��1��c(NH3)��4.00 mol��L��1�����¶��¸÷�Ӧ��ƽ�ⳣ��K��________��
(2)��������ͬ�����и�����1 mol N2��3 mol H2���ڲ�ͬ�����·�Ӧ���ﵽƽ�⣬�������������ʱ��仯��������ͼ��ʾ������˵������ȷ����________(����ĸ)��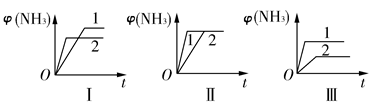
| A��ͼ������Dz�ͬѹǿ�Է�Ӧ��Ӱ�죬��p2>p1 |
| B��ͼ������Dz�ͬѹǿ�Է�Ӧ��Ӱ�죬��p1>p2 |
| C��ͼ������Dz�ͬ�¶ȶԷ�Ӧ��Ӱ�죬��T1>T2 |
| D��ͼ�������ͬ��ͬѹ�²�ͬ�����Է�Ӧ��Ӱ�죬�Ҵ�������1>2 |
��H����131.3 kJ��mol��1����S����133.7J��K��1 ��mol��1
�÷�Ӧ�ڳ������ܷ��Է����У�________(��ܡ����ܡ�)��
 xC(g)���ڲ�ͬ������������C�ڷ�Ӧ������е���������(C%)�ͷ�Ӧʱ��(t)�Ĺ�ϵ����ͼ��
xC(g)���ڲ�ͬ������������C�ڷ�Ӧ������е���������(C%)�ͷ�Ӧʱ��(t)�Ĺ�ϵ����ͼ��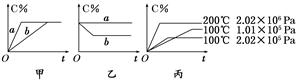
 yC(g)����H��0����һ�������£�������A��C�����ʵ���Ũ����ʱ��仯��������ͼ��ʾ����ش��������⣺
yC(g)����H��0����һ�������£�������A��C�����ʵ���Ũ����ʱ��仯��������ͼ��ʾ����ش��������⣺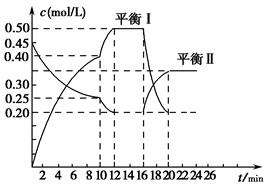
 CO2(g)��H2(g)����Ӧ�ų���������Ӧ��CO2��Ũ����ʱ��仯�������ͼ��ʾ��
CO2(g)��H2(g)����Ӧ�ų���������Ӧ��CO2��Ũ����ʱ��仯�������ͼ��ʾ��