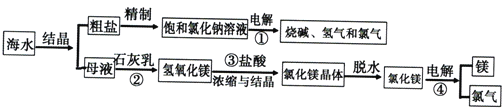
题目内容
【题目】下图是实验室制备气体常用的装置图,请回答下面相关问题:
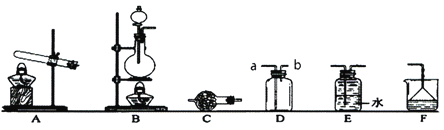
(1)①实验室用Na2SO3与浓硫酸反应制备SO2,应该选取_____装置(填写“A”或“B”),多余的SO2气体需要通过F装置吸收,装置中倒置的漏斗作用是_______。
②若采用D装置收集SO2气体,则进气管应该接______(填写“a”或“b”)
(2)①若选取A装置制备氨气,该反应的化学方程式为_________。
②干燥氨气时,常常在装置C中加入_______作干燥剂。
③有人说可以使用装置E收集氨气,你认为该观点是否正确?_______(填写“正确”或“不正确”) ,请说出原因______________。
【答案】B防倒吸a2NH4Cl +Ca(OH)2![]() CaCl2 +H2O +2NH3↑碱石灰(其它合理答案也可)不正确因为氨气极易溶解于水(其它合理说法也可)
CaCl2 +H2O +2NH3↑碱石灰(其它合理答案也可)不正确因为氨气极易溶解于水(其它合理说法也可)
【解析】
(1). ①A装置适用于固体加热制备气体的反应,B装置适用于固体和液体加热制备气体的反应,所以选B ; 多余的二氧化硫一般用氢氧化钠溶液吸收,二氧化硫在氢氧化钠溶液中的溶解度很大,直接用玻璃导管通入其中引起倒吸,所以用小漏斗倒扣于液面防倒吸 ②二氧化硫气体可用向上排空气法收集,气体应长进短出,所以选a
(2). ①实验室用氯化铵和氢氧化钙加热制备氨气:2NH4Cl +Ca(OH)2![]() CaCl2 +H2O +2NH3↑ ,②氨气的水溶液显碱性,常用碱性干燥剂干燥,所以用碱石 灰 ③氨气极易溶于水,不能用排水集气法收集氨气,所以不正确 。
CaCl2 +H2O +2NH3↑ ,②氨气的水溶液显碱性,常用碱性干燥剂干燥,所以用碱石 灰 ③氨气极易溶于水,不能用排水集气法收集氨气,所以不正确 。

 阅读快车系列答案
阅读快车系列答案【题目】如图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略)
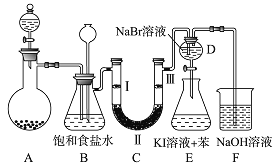
(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的离子反应方程式为:_____________.装置 B 中饱和食盐水的作用是_________________;
若C处发生了堵塞,则B中的现象为__________________.
(2)装置 C 的实验目的是验证氯气是否具有漂白性,为此 C 中Ⅰ、Ⅱ、Ⅲ应该依次放入____(填编号)
① | ② | ③ | ④ | |
I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(3)设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱。当向D中缓缓通入少量氯气时,可以看到无色溶液逐渐变为______色,说明________________;打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是__________________;
(4)如果将二氧化锰与足量的浓盐酸混合加热,若有17.4g 的 MnO2 被还原,则被氧化的 HCl 的质量为_____.
(5)向 Na2CO3 溶液中通入氯气,可制得某种生产和生活中常用的漂白液,同时有 NaHCO3 生成,该反应的化学方程式是______.