题目内容
某溶液,只可能含有以下离子中的若干种:H+、NH4+、K+、Mg2+、NO2-、CO32-、NO3-,现取两份100mL溶液进行如下实验:
①第一份加足量AgNO3溶液后,有5.84g白色沉淀产生,沉淀中加入足量稀盐酸充分反应,有棕色气体产生,沉淀颜色不变,但是质量减少0.1g;
②将产生的气体全部通入过量的澄清石灰水,又得到白色沉淀1.0g,该沉淀能溶于稀盐酸产生无色气体;
③第二份加入过量浓NaOH溶液,加热使产生的气体全部放出,用50mL0.5mol·L-1的硫酸溶液恰好完全吸收,酸也不剩余。
根据上述实验,以下推测不正确的是( )
| A.原溶液一定不存在较大浓度的H+、Mg2+ |
| B.原溶液确定含NH4+、NO2-、CO32-,且物质的量之比为5︰2︰1 |
| C.不能确定原溶液是否含有K+、NO3- |
| D.实验中产生的棕色气体遇空气颜色会加深 |
C
解析试题分析:第一份加足量AgNO3溶液后,有5.84g白色沉淀产生,沉淀中加入足量稀盐酸充分反应,有棕色气体产生,沉淀颜色不变,但是质量减少0.1g,这说明该白色沉淀中一定含有亚硝酸银,亚硝酸银与盐酸反应生成氯化银与亚硝酸,亚硝酸不稳定分解生成NO、NO2和水。所以原溶液中一定含有NO2-,则氢离子一定不能大量共存。将产生的气体全部通入过量的澄清石灰水,又得到白色沉淀1.0g,该沉淀能溶于稀盐酸产生无色气体,则该白色沉淀应该是碳酸钙,物质的量是0.01mol,所以气体中含有CO2,这说明反应①中生成的白色沉淀一定有碳酸银,则原溶液中一定含有CO32-。因此Mg2+就一定不能大量共存。根据碳原子守恒,CO32-的物质的量是0.01mol。5.84g沉淀中亚硝酸银沉淀的质量=5.84g-0.01mol×276g/mol=3.08g,因此亚硝酸银的物质的量=3.08g÷154g/mol=0.02mol,则原溶液中NO2-的物质的量是0.02mol。第二份加入过量浓NaOH溶液,加热使产生的气体全部放出,该气体一定是氨气,因此原溶液中含有NH4+。用50mL0.5mol/L的硫酸溶液恰好完全吸收,酸也不剩余,硫酸的物质的量是0.025mol,则氨气的物质的量是0.025mol×2=0.05mol,则原溶液中NH4+的物质的量是0.05mol,所以原溶液确定含NH4+、NO2-、CO32-,且物质的量之比为5︰2︰1,因此选项A、B正确。根据电荷守恒可知,原溶液中一定还含有NO3-,但K+不能确定,C不正确;实验中产生的棕色气体中含有NO,遇空气生成红棕色NO2,所以颜色会加深,D正确,答案选C。
考点:考查考查离子共存、离子检验的有关判断

 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案某无色溶液中可能含有I-、K+、Cu2+、SO32-(还原性:SO32->I-),向该溶液中加入少量
溴水,溶液仍呈无色,则下列关于溶液组成的判断正确的是
①肯定不含I-; ②肯定不含Cu2+; ③肯定含有SO32-; ④可能含有I-。
| A.①③ | B.①②③ | C.②③④ | D.①② |
常温下,下列各组离子在指定溶液中能大量共存的是
| A.pH=13的溶液中:Na+、CO32―、Al3+、ClO― |
| B.c(H+)/c(OH―) =1010的溶液中:K+、Fe2+、Cl―、SO42― |
| C.加入铝片能放出H2的溶液中:Na+、HCO3―、Cu2+、SO42― |
| D.水电离出来的c(H+)=10-13mol·L-1的溶液中:NH4+、K+、NO3―、SiO32― |
下列实验过程中产生的现象与所给图形相符合的是( )
| A.往乙酸中通入氨气 |
B.往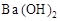 溶液中滴加硫酸 溶液中滴加硫酸 |
| C.往氢硫酸溶液中通入氯气 |
| D.往NaOH溶液中通入过量CO2 |
下列离子方程式书写正确的是
| A.将过量的NaOH溶液滴入同浓度的少量Ca(HCO3)2溶液中Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32- |
| B.向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全Ba2++OH-+H++ SO42-=BaSO4↓+H2O |
C.服用阿司匹林过量出现水杨酸( )反应,可静脉注滴NaHCO3溶液: )反应,可静脉注滴NaHCO3溶液: + 2 HCO3- → + 2 HCO3- → + 2 CO2↑ + 2 H2O + 2 CO2↑ + 2 H2O |
| D.向FeI2溶液中加少量氯水 2Fe2++Cl2=2Fe3++2Cl- |
某溶液仅含Fe2+、Na+、Al3+、Ba2-、SO42-、NO3-、Cl-中的4种离子,所含离子的物质的量均为1mol.若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。下列说法不正确的是
| A.若向该溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为7.2克 |
| B.若向该溶液中加入足量的稀硫酸,产生的气体遇空气能变成红棕色 |
| C.若向该溶液中加入足量的稀硫酸和KSCN溶液,溶液显血红色 |
| D.该溶液中所含的离子是:Fe2+、Na+、SO42-、NO3- |
下列离子或分子在溶液中能大量共存,通入CO2后仍能大量共存的一组是
| A.K+、Na+、Br-、SiO32- | B.K+、Na+、Cl-、NO3- |
| C.H+、Fe2+、SO42-、Cl2 | D.K+、Ag+、NH3·H2O、NO3- |
下列反应一定有沉淀生成的是
| A.将SO2通入BaCl2溶液中 | B.将NH3通入AgNO3溶液中 |
| C.将Cl2通入AgNO3溶液中 | D.将NO2通入Ca(OH)2溶液中 |
下列离子方程式书写正确的是
A.向海带灰浸出液中加入硫酸、双氧水:2I-+2H++H2O2 I2+2H2O I2+2H2O |
B.Cu片插入FeCl3溶液中:Cu+Fe3+ Fe2++Cu2+ Fe2++Cu2+ |
C.向Al2(SO4)3溶液中加入过量的氨水: Al3++4NH3·H2O  AlO2-+4NH4++2H2O AlO2-+4NH4++2H2O |
| D.向 NaHSO4溶液中滴加Ba(OH)2溶液至中性: |
 BaSO4↓+H2O
BaSO4↓+H2O