题目内容
下列装置所示的实验不能达到目的是( )
A、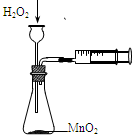 定量测定化学反应速率 |
B、 验证Na和水反应的热效应 |
C、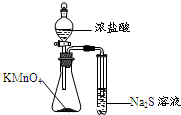 比较KMnO4、Cl2、S的氧化性 |
D、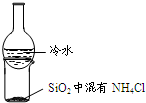 加热烧杯,分离SiO2和NH4Cl |
考点:化学实验方案的评价,氧化性、还原性强弱的比较,物质的分离、提纯的基本方法选择与应用,测定某些化学反应的速率,碱金属及其化合物的性质实验
专题:实验评价题
分析:A.该实验中用分液漏斗盛放双氧水;
B.利用气体热胀冷缩性质确定钠和水反应的反应热;
C.同一氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性;
D.氯化铵加热易分解生成氨气和氯化氢,氨气和氯化氢遇冷生成氯化铵.
B.利用气体热胀冷缩性质确定钠和水反应的反应热;
C.同一氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性;
D.氯化铵加热易分解生成氨气和氯化氢,氨气和氯化氢遇冷生成氯化铵.
解答:
解:A.该实验中用分液漏斗盛放双氧水,如果用长颈漏斗易导致生成的气体从漏掉中逸出,故A错误;
B.空气有热胀冷缩的性质,如果钠和水的反应放出热量,会导致大试管中空气膨胀,压强增大,导致U型管中红墨水左低右高,所以能实现实验目的,故B正确;
C.同一氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性,浓盐酸被高锰酸钾氧化生成氯气,氯气氧化硫化钠生成S单质,所以氧化性KMnO4>Cl2>S,故C正确;
D.氯化铵加热易分解生成氨气和氯化氢,氨气和氯化氢遇冷生成氯化铵,加热时二氧化硅不分解,所以能分离两种物质,故D正确;
故选A.
B.空气有热胀冷缩的性质,如果钠和水的反应放出热量,会导致大试管中空气膨胀,压强增大,导致U型管中红墨水左低右高,所以能实现实验目的,故B正确;
C.同一氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性,浓盐酸被高锰酸钾氧化生成氯气,氯气氧化硫化钠生成S单质,所以氧化性KMnO4>Cl2>S,故C正确;
D.氯化铵加热易分解生成氨气和氯化氢,氨气和氯化氢遇冷生成氯化铵,加热时二氧化硅不分解,所以能分离两种物质,故D正确;
故选A.
点评:本题考查了实验方案评价,涉及氧化性强弱比较、反应热、除杂、反应速率的测定等知识点,明确实验原理及物质的性质是解本题关键,注意C中生成的氯气中含有HCl,但HCl不氧化硫化钠,从而不影响实验目的,为易错点.

练习册系列答案
相关题目
下列电离方程式正确的是( )
| A、Cu(OH)2?Cu2++2OH- |
| B、NaHCO3=Na++H++CO32- |
| C、CH3COOH=CH3COO-+H+ |
| D、H2S?2H++S2- |
在酸性高锰酸钾溶液中加入过氧化钠粉末,溶液褪色,其中发生反应的离子方程式为:2MnO4-+16H++5Na2O2═2Mn2++5O2↑+8H2O+10Na+.下列判断正确的是( )
| A、Na2O2既是氧化剂,又是还原剂 |
| B、O2是还原产物,Mn2+是氧化产物 |
| C、通常用浓盐酸酸化高锰酸钾溶液 |
| D、标准状况下,产生22.4L O2时反应转移2mol e- |
下列表示对应化学反应的离子方程式不正确的是( )
| A、FeCl3溶液与Cu的反应:Cu+2Fe3+═Cu2++2Fe2+ |
| B、向NaClO溶液中加入浓盐酸:ClO-+Cl-+2H+═Cl2↑+H2O |
| C、用氨水溶解Cu(OH)2:Cu(OH)2+4NH3?H2O═[Cu(NH3)4]2++2OH-+4H2O |
| D、向NH4HCO3中滴加少量的NaOH溶液:NH4++OH-═NH3?H2O+H2O |
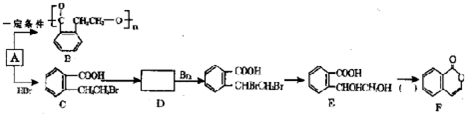
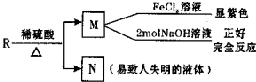
 下图表示的反应关系中,部分产物被略去.已知2mol白色固体粉末受热分解,恢复到室温生成白色固体A、无色液体B、无色气体C各1mol.X、E、G的焰色反应均为黄色.
下图表示的反应关系中,部分产物被略去.已知2mol白色固体粉末受热分解,恢复到室温生成白色固体A、无色液体B、无色气体C各1mol.X、E、G的焰色反应均为黄色.