��Ŀ����
 ��ͼ��ʾ�ķ�Ӧ��ϵ�У����ֲ��ﱻ��ȥ����֪2mol��ɫ�����ĩ���ȷֽ⣬�ָ����������ɰ�ɫ����A����ɫҺ��B����ɫ����C��1mol��X��E��G����ɫ��Ӧ��Ϊ��ɫ��
��ͼ��ʾ�ķ�Ӧ��ϵ�У����ֲ��ﱻ��ȥ����֪2mol��ɫ�����ĩ���ȷֽ⣬�ָ����������ɰ�ɫ����A����ɫҺ��B����ɫ����C��1mol��X��E��G����ɫ��Ӧ��Ϊ��ɫ���ش��������⣺
��1��д���������ʵĻ�ѧʽ��G
��2��д��G�������C��Ӧ����D�Ļ�ѧ��Ӧ����ʽ��
��3��д��X+E��A�����ӷ���ʽ��
��4��д��C��Na2O2�μӷ�Ӧ�Ļ�ѧ����ʽ��
���㣺������ƶ�
ר�⣺�ƶ���
������X��E��G����ɫ��Ӧ��Ϊ��ɫ��������NaԪ�أ�X�ֽ�������ɫҺ��B����BΪH2O����֪EΪNaOH��GΪNaAlO2����ɫ����C��Na2O2��Ӧ���ɰ�ɫ����A��CΪCO2��A��Na2CO3��CO2+NaAlO2��D����DΪAl��OH��3��2mol��ɫ�����ĩX���ȷֽ⣬����1molNa2CO3��1molH2O��1molCO2������Ԫ���غ��֪��XΪNaHCO3��X��NaOH��Ӧ����Na2CO3����EΪNaOH��NaHCO3+F��CO2��F������������εȣ�
���
�⣺X��E��G����ɫ��Ӧ��Ϊ��ɫ��������NaԪ�أ�X�ֽ�������ɫҺ��B����BΪH2O����֪EΪNaOH��GΪNaAlO2����ɫ����C��Na2O2��Ӧ���ɰ�ɫ����A��CΪCO2��A��Na2CO3��CO2+NaAlO2��D����DΪAl��OH��3��2mol��ɫ�����ĩX���ȷֽ⣬����1molNa2CO3��1molH2O��1molCO2������Ԫ���غ��֪��XΪNaHCO3��X��NaOH��Ӧ����Na2CO3����EΪNaOH��NaHCO3+F��CO2��F������������Σ�
��1��������������֪��GΪNaAlO2��DΪAl��OH��3��
�ʴ�Ϊ��NaAlO2��Al��OH��3��
��2����ƫ��������Һ��ͨ������Ķ�����̼����Ӧ������������������̼�����ƣ���ѧ��Ӧ����ʽΪ��NaAlO2+CO2+2H2O=Al��OH��3��+NaHCO3��
�ʴ�Ϊ��NaAlO2+CO2+2H2O=Al��OH��3��+NaHCO3��
��3��X+E��A��NaHCO3��NaOH��Ӧ����Na2CO3��H2O����Ӧ���ӷ���ʽΪ��HCO3-+OH-=CO32-+H2O��
�ʴ�Ϊ��HCO3-+OH-=CO32-+H2O��
��4��CΪCO2����������Ʒ�Ӧ����̼��������������Ӧ����ʽΪ��2Na2O2+2CO2=2Na2CO3+O2��
�ʴ�Ϊ��2Na2O2+2CO2=2Na2CO3+O2��
��1��������������֪��GΪNaAlO2��DΪAl��OH��3��
�ʴ�Ϊ��NaAlO2��Al��OH��3��
��2����ƫ��������Һ��ͨ������Ķ�����̼����Ӧ������������������̼�����ƣ���ѧ��Ӧ����ʽΪ��NaAlO2+CO2+2H2O=Al��OH��3��+NaHCO3��
�ʴ�Ϊ��NaAlO2+CO2+2H2O=Al��OH��3��+NaHCO3��
��3��X+E��A��NaHCO3��NaOH��Ӧ����Na2CO3��H2O����Ӧ���ӷ���ʽΪ��HCO3-+OH-=CO32-+H2O��
�ʴ�Ϊ��HCO3-+OH-=CO32-+H2O��
��4��CΪCO2����������Ʒ�Ӧ����̼��������������Ӧ����ʽΪ��2Na2O2+2CO2=2Na2CO3+O2��
�ʴ�Ϊ��2Na2O2+2CO2=2Na2CO3+O2��
����������������ͼ�����ʽ���������ƶϣ��漰Na��Al��Ԫ�ص��ʼ���������ת����ϵ������ɫҺ��B��X��E��G����ɫ��Ӧ��Ϊ��ɫ�����ǽ���ͻ�ƿڣ��������C��Na2O2��Ӧ����˳�Ʒ������Ʒ������ƶϣ��Ѷ��еȣ�

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
1.1mol������������ȫ��Ӧ�������Ȼ������Ȼ��ף������ʵ�����Ϊ2��1���������������Ȼ������ʵ���Ϊ��������
| A��0.4mol |
| B��0.1mol |
| C��0.2mol |
| D��0.05mol |
����װ����ʾ��ʵ�鲻�ܴﵽĿ���ǣ�������
A��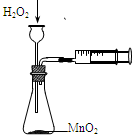 �����ⶨ��ѧ��Ӧ���� |
B�� ��֤Na��ˮ��Ӧ����ЧӦ |
C��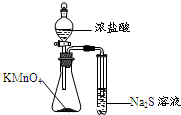 �Ƚ�KMnO4��Cl2��S�������� |
D��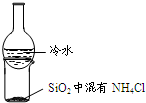 �����ձ�������SiO2��NH4Cl |
| 1 |
| 28 |
A��
| ||
| B��14x mol-1 | ||
| C��28x mol-1 | ||
| D��28x |

