题目内容
运用元素周期律分析下面推断,其中错误的是
| A.铍(Be)的氧化物的水化物可能具有两性 |
| B.砹(At)为有色固体,HAt不稳定,A gAt感光性很强 ,但不溶于水也不溶于酸 |
| C.硫酸锶(SrSO4)是难溶于水的白色固体 |
| D.硒化氢(H2Se)是有色、有毒的气体,比H2S稳定 |
D
试题分析:A:元素周期表中的对角线规则:处于对角线的元素具有相似性,铍(Be)的氧化物的水化物和铝的氧化物的水化物氢氧化铝性质相似,可能具有两性,A正确;B:同主族元素性质具有相似性,根据卤族元素但只以及银盐的性质,可以推知砹(At)为有色固体,HAt不稳定,AgAt感光性很强,但不溶于水也不溶于稀酸,B正确;C:根据第ⅡA元素硫酸盐性质的递变规律,可以知道硫酸锶(SrSO4)是难溶于水的白色固体;D:同主族元素的原子,从上到下氢化物的稳定性逐渐减弱,硒化氢(H2Se)是无色,有毒,不如H2S稳定的气体,D错,故选D
点评:本题考查元素周期表中同周期和同主族元素的性质变化规律,学生明确金属性与非金属性强弱的比较方法是解答本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
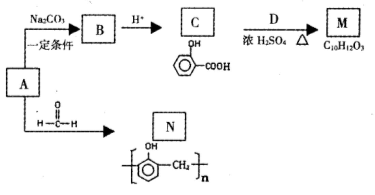
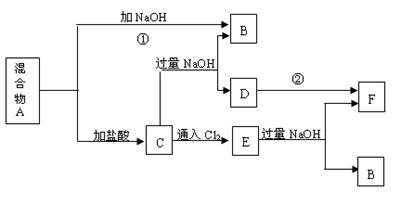
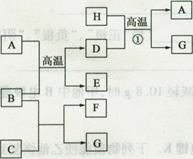

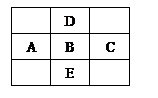

 能放出大量的热,该反应曾应用于铁轨的焊接;
能放出大量的热,该反应曾应用于铁轨的焊接; 可以发生反应:2E+I
可以发生反应:2E+I 2F+D,F中的E元素的质量分数为60%.
2F+D,F中的E元素的质量分数为60%.