题目内容
【题目】下图是实验室制取SO2并验证SO2的某些性质的装置,请回答:
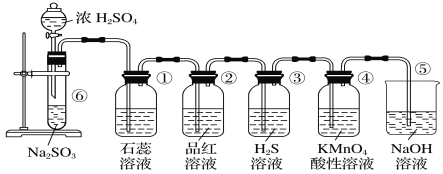
(1)在⑥中发生反应的化学方程式为______________________________________。
(2)①中的实验现象为石蕊溶液____________,此实验证明SO2具有____________的性质。
(3)②中的品红溶液________,证明SO2有________性。
(4)③中的实验现象是________________________,证明SO2有____________性。
(5)④中的实验现象是______,证明SO2有______性。
(6)⑤的作用是____________,反应的化学方程式为____________ 。
【答案】Na2SO3+H2SO4(浓) ===Na2SO4+H2O+SO2↑ 变红 酸性 褪色 漂白 有淡黄色沉淀生成 氧化 高锰酸钾溶液褪色 还原 吸收二氧化硫,防止二氧化硫污染环境 SO2+2NaOH===Na2SO3+H2O
【解析】
(1)亚硫酸钠与浓硫酸反应生成二氧化硫、硫酸钠和水;
(2)二氧化硫溶于水和水反应生成亚硫酸,亚硫酸可以使紫色石蕊试液变红;
(3)根据二氧化硫具有漂白性分析;
(4)根据二氧化硫具有氧化性,H2S具有还原性分析;
(5)根据二氧化硫具有还原性分析;
(6)二氧化硫有毒,不能直接排放到空气中,为酸性氧化物能够与氢氧化钠反应生成亚硫酸钠和水。
(1)⑥中为亚硫酸钠和浓硫酸反应生成二氧化硫气体,反应的化学方程式为Na2SO3+H2SO4(浓)=Na2SO4+H2O+SO2↑;
(2)二氧化硫溶于水和水反应生成亚硫酸,亚硫酸为二元中强酸,可以使紫色石蕊试液变红,即①中的实验现象为紫色石蕊试液变红,此实验证明二氧化硫是酸性气体;
(3)二氧化硫与品红化合生成无色物质,能使品红溶液褪色,故二氧化硫具有漂白性;
(4)SO2中+4价S具有氧化性,硫化氢中-2价S具有还原性,二氧化硫能把硫化氢氧化成单质硫,本身被还原成单质硫,反应方程式为SO2+2H2S=3S↓+2H20,所以③中的实验现象是有淡黄色沉淀生成;
(5)二氧化硫具有还原性,能被酸性高锰酸钾溶液氧化而使其褪色;
(6)二氧化硫有毒,不能直接排放到空气中,二氧化硫能够与氢氧化钠反应生成亚硫酸钠和水,所以可以用氢氧化钠溶液吸收二氧化硫,即⑤的作用是吸收二氧化硫,防止二氧化硫污染环境,反应的化学方程式为SO2+2NaOH=Na2SO3+H2O。

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案【题目】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) ![]() CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
t ℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=_________________________________。
(2)该反应为________反应(填“吸热”或“放热”)。
(3)某温度下,各物质的平衡浓度符合下式:3c(CO2)·c(H2)=5c(CO)·c(H2O),试判断此时的温度为______。
(4)若830 ℃时,向容器中充入1 mol CO、5 mol H2O,反应达到平衡后,其化学平衡常数K______1.0(填“大于”“小于”或“等于”)。
(5)830 ℃时,容器中的反应已达到平衡。在其他条件不变的情况下,扩大容器的体积。平衡____移动(填“向正反应方向”“向逆反应方向”或“不”)。
(6)若1 200 ℃时,在某时刻平衡体系中CO2、H2、CO、H2O的浓度分别为2 mol·L-1、2 mol·L-1、4 mol·L-1、4 mol·L-1,则此时上述反应的平衡移动方向为__________(填“正反应方向”“逆反应方向”或“不移动”)。