题目内容
甲醇是一种可再生的优质燃料,用途广泛,研究其作用具有广阔前景。
(1)已知在常温常压下,测得反应的反应热如下:
① 2CH3OH(l)+ 3O2(g) 2CO2(g) +4H2O(g) ?H1= -1275.6 kJ/mol
2CO2(g) +4H2O(g) ?H1= -1275.6 kJ/mol
② 2CO(g) +O2(g) 2CO2(g) ?H2=-566.0 kJ/mol
2CO2(g) ?H2=-566.0 kJ/mol
CH3OH不完全燃烧生成CO和气态水的热化学方程式是 。
(2)工业上生产甲醇的反应如下:CO2(g) + 3H2(g) CH3OH(g)+ H2O(g) ?H = -49 kJ/mol
CH3OH(g)+ H2O(g) ?H = -49 kJ/mol
在某温度下,容积均为1 L的A、B两个容器中,按不同方式投入反应物,保持恒温恒容。容器B中经10 s后达到平衡。达到平衡时的有关数据如下表:
①从反应开始至达到平衡时,容器B中CH3OH的平均反应速率为 。
②该温度下,B容器中反应的化学平衡常数的数值为 。
③α= 。
④下列措施能使容器A中甲醇的产率增大的是 。
a.升高温度 b.将水蒸气从体系分离
c.用更有效的催化剂 d.将容器的容积缩小一半
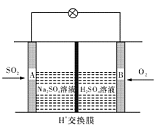
(3)我国科学院化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池。甲醇燃料电池的工作原理如下图所示。

① 该电池工作时,b口通入的物质为 。
② 该电池正极的电极反应式为 。
(1)已知在常温常压下,测得反应的反应热如下:
① 2CH3OH(l)+ 3O2(g)
 2CO2(g) +4H2O(g) ?H1= -1275.6 kJ/mol
2CO2(g) +4H2O(g) ?H1= -1275.6 kJ/mol ② 2CO(g) +O2(g)
 2CO2(g) ?H2=-566.0 kJ/mol
2CO2(g) ?H2=-566.0 kJ/molCH3OH不完全燃烧生成CO和气态水的热化学方程式是 。
(2)工业上生产甲醇的反应如下:CO2(g) + 3H2(g)
 CH3OH(g)+ H2O(g) ?H = -49 kJ/mol
CH3OH(g)+ H2O(g) ?H = -49 kJ/mol 在某温度下,容积均为1 L的A、B两个容器中,按不同方式投入反应物,保持恒温恒容。容器B中经10 s后达到平衡。达到平衡时的有关数据如下表:
| 容器 | A | B |
| 反应物投入量 | 1 mol CO2(g)和3 mol H2(g) | 1 mol CH3OH(g)和1 mol H2O(g) |
| 反应能量变化 | 放出αkJ热量 | 吸收19.6 kJ热量 |
①从反应开始至达到平衡时,容器B中CH3OH的平均反应速率为 。
②该温度下,B容器中反应的化学平衡常数的数值为 。
③α= 。
④下列措施能使容器A中甲醇的产率增大的是 。
a.升高温度 b.将水蒸气从体系分离
c.用更有效的催化剂 d.将容器的容积缩小一半
(3)我国科学院化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池。甲醇燃料电池的工作原理如下图所示。

① 该电池工作时,b口通入的物质为 。
② 该电池正极的电极反应式为 。
(1)CH3OH(l)+ O2(g)  CO (g) +2H2O(g) ?H= -354.8 kJ/mol(2分)
CO (g) +2H2O(g) ?H= -354.8 kJ/mol(2分)
(2)① 0.04 mol/L·S (2分)
② 1.92 (2分)
③ 29.4 kJ (1分)
④ b d (1分)
(3)① CH3OH (1分)
② O2+4e-+4H+ 2H2O(1分)
2H2O(1分)
 CO (g) +2H2O(g) ?H= -354.8 kJ/mol(2分)
CO (g) +2H2O(g) ?H= -354.8 kJ/mol(2分)(2)① 0.04 mol/L·S (2分)
② 1.92 (2分)
③ 29.4 kJ (1分)
④ b d (1分)
(3)① CH3OH (1分)
② O2+4e-+4H+
 2H2O(1分)
2H2O(1分)试题分析:(1)CH3OH不完全燃烧生成CO和气态水的热化学方程式用(①-②)÷2即得,所以答案是CH3OH(l)+ O2(g)
 CO (g) +2H2O(g) ?H= -354.8 kJ/mol;
CO (g) +2H2O(g) ?H= -354.8 kJ/mol;(2)①达平衡时,B容器的热效应是吸收 19.6 kJ热量,即甲醇的物质的量减少19.6/49=0.4mol,浓度减少0.4mol/L,所以容器B中CH3OH的平均反应速率为0.4mol/L/10s=0.04 mol/L·S
②B容器中平衡时c(CH3OH)=1-0.4=0.6mol/L=c(H2O),c(CO2)=0.4 mol/L ,c(H2)=1.2 mol/L,所以B容器的化学平衡常数K= c(CO2) c(H2)3/ c(CH3OH) c(H2O)=1.92
③a容器的化学平衡常数是1/1.92,设平衡时甲醇的浓度为x,则1/1.92=x2/(1-x)(3-3x)3,解得x=0.6mol/L,所以α=0.6mol/L×1L×49 kJ/mol =29.4 kJ
④a、升高温度,平衡逆向移动,甲醇产率减少,错误;b、将水蒸气从体系分离,生成物浓度减小,平衡正向移动,甲醇产率增大,正确;c、使用催化剂对平衡无影响,错误;d、将容器的容积缩小一半,压强增大,平衡正向移动,甲醇产率增大,正确,答案选bd。
(3)原电池中阳离子移向正极,所以电池右侧为正极,氧气发生还原反应,电极反应式为O2+4e-+4H+
 2H2O,所以电池左侧为负极,b口应通CH3OH。
2H2O,所以电池左侧为负极,b口应通CH3OH。
练习册系列答案
相关题目
 时:
时:


 C6 H5- CH=CH2 (g) +H2(g) ΔH1
C6 H5- CH=CH2 (g) +H2(g) ΔH1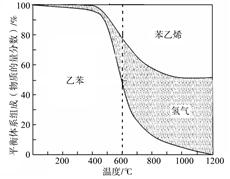



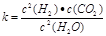 它所对应的化学反应为:__ ___
它所对应的化学反应为:__ ___ CH3OCH3(g)+ 3H2O(g)
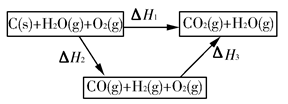
CH3OCH3(g)+ 3H2O(g) CO(g)+H2(g);②C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:
CO(g)+H2(g);②C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为: