题目内容
【题目】苯环中不存在碳碳单键和碳碳双键交替的结构,可以作为证据的事实是( )
①苯是无色易挥发的液体;
②苯不能使酸性高锰酸钾溶液褪色;
③![]() 和
和 是同一种物质。
是同一种物质。
A. ①②③ B. ①和② C. ①和③ D. ②和③
【答案】D
【解析】如存在碳碳双键,可发生加成反应、氧化反应,且邻二代物存在同分异构体,以此解答该题。
①苯是无色易挥发的液体属于物理性质,不能证明苯的结构,①错误;
②苯不能使酸性高锰酸钾溶液褪色,说明苯分子中不含碳碳双键,可以证明苯环结构中不存在碳碳单键与碳碳双键的交替结构,②正确;
③如果是单双键交替结构,邻二甲苯的结构有两种,由于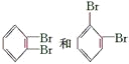 是同一种物质,说明苯环结构中的化学键只有一种,不存在碳碳单键与碳碳双键的交替结构,③正确;
是同一种物质,说明苯环结构中的化学键只有一种,不存在碳碳单键与碳碳双键的交替结构,③正确;
所以②③可以作为苯分子中不存在单、双键交替排列结构的证据。答案选D。

【题目】下列根据实验操作和现象所得出的结论正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 将SO2气体通入Ba(NO3)2溶液 | 有白色沉淀 | SO2中混有SO3 |
B | 向NaAlO2溶液中持续通入气体Y | 先出现白色沉淀,最终沉淀又溶解 | Y可能是CO2气体 |
C | AgCl悬浊液中滴入少量Na2S溶液 | 沉淀变黑色 | Ksp(Ag2S)>Ksp(AgCl) |
D | 向盛有KI3溶液的两试管中分别加入淀粉溶液和AgNO3溶液 | 前者溶液变蓝色,后者有黄色沉淀 | KI3溶液中存在平衡: I3- |
A. A B. B C. C D. D
【题目】电解质的水溶液中存在电离平衡.
(1)醋酸是常见的弱酸. ①醋酸在水溶液中的电离方程式为 .
②下列方法中,可以使醋酸稀溶液中CH3COOH电离程度增大的是(填字母序号).
A.滴加少量浓盐酸 B.微热溶液
C.加水稀释 D.加入少量醋酸钠晶体
(2)用0.1molL﹣1NaOH溶液分别滴定体积均为20.00mL、浓度均为0.1molL﹣1的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线. 
①滴定醋酸的曲线是(填“I”或“Ⅱ”).
②滴定开始前,三种溶液中由水电离出的c(H+)最大的是 .
③V1和V2的关系:V1V2(填“>”、“=”或“<”).
④M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是 .
(3)为了研究沉淀溶解平衡和沉淀转化,某同学查阅资料并设计如下实验. 资料:AgSCN是白色沉淀,相同温度下,溶解度:AgSCN>AgI.
操作步骤 | 现象 |
步骤1:向2mL 0.005molL﹣1 AgNO3溶液中加入2mL 0.005molL﹣1 KSCN溶液,静置 | 出现白色沉淀 |
步骤2:取1mL上层清液于试管中,滴加1滴2molL﹣1 Fe(NO3)3溶液 | 溶液变红色 |
步骤3:向步骤2的溶液中,继续加入5滴3molL﹣1 AgNO3溶液 | 现象a﹍﹍﹍,溶液红色变浅 |
步骤4:向步骤1余下的浊液中加入5滴3molL﹣1 KI溶液 | 出现黄色沉淀 |
①写出步骤2中溶液变红色的离子方程式 .
②步骤3中现象a是 .
③用化学平衡原理解释步骤4的实验现象 .