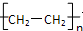题目内容
9.乙酸是生活中常见的有机物,下列说法不正确的是( )| A. | 食醋中含有3-5%的乙酸 | B. | 乙酸可被催化氧化成乙醛 | ||
| C. | 可用乙酸清除水壶中的水垢 | D. | 乙酸分子的官能团是-COOH |
分析 A、乙酸是食醋的主要成分;
B、乙酸除了燃烧,不能被氧化;
C、乙酸的酸性强于碳酸,根据强酸制弱酸的原理来分析;
D、羧酸的官能团为羧基.
解答 解:A、乙酸是食醋的主要成分,食醋中含3-5%的乙酸,故A正确;
B、乙酸除了燃烧,不能被氧化,且恰好相反,是乙醛能被氧化为乙酸,故B错误;
C、乙酸的酸性强于碳酸,根据强酸制弱酸的原理可知,乙酸能和水垢中的CaCO3、Mg(OH)2反应,从而能去水垢,故C正确;
D、羧酸的官能团为羧基,结构简式为-COOH,故D正确.
故选B.
点评 本题考查了乙酸的用途和性质,难度不大,应注意的是乙酸的酸性强于碳酸.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
20.下列反应的离子方程式书写正确的是( )
| A. | Ba(OH)2溶液与稀硫酸反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O | |
| B. | 用醋酸溶解石灰石:CaCO3+2CH3COOH═Ca2++H2O+CO2↑+2CH3COO- | |
| C. | (NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-=Fe(OH)2↓ | |
| D. | Cu溶于稀硝酸:Cu+2H++NO3=Cu2++NO2↑+H2O |
4.A、B均为短周期主族元素,A原子的最外层有2个电子,B原子的最外层有7个电子,这两种元素形成化合物的化学式是( )
| A. | AB2 | B. | A2B | C. | AB | D. | A2B3 |
14.下列物质中既有离子键又有共价键的是( )
| A. | KCl | B. | SiO2 | C. | Na2O2 | D. | HNO3 |
1.符合分子式C5H8O4的所有同分异构体在下列一种表征仪器显示的信号(或数据)完全相同,该仪器是( )
| A. | 元素分析仪 | B. | 红外光谱仪 | C. | 质谱仪 | D. | 核磁共振仪 |
19.下列溶液中,溶质的物质的量浓度为1mol/L的是( )
| A. | 将40 g NaOH溶于1 L水所得的溶液 | |
| B. | 将80 g SO3溶于水并配成1 L的溶液 | |
| C. | 将0.5 mol/L的NaNO3溶液100 mL加热蒸发掉50 g水的溶液 | |
| D. | 含K+为2 mol的K2SO4溶液 |