题目内容
一定条件下,溶液的酸碱性对TiO2光催化染料R降解反应的影响如图所示.下列判断正确的是( )
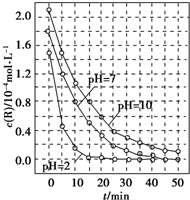

| A、在0-50 min之间,pH=2和PH=7时R的降解百分率不相等 |
| B、在20-25 min之间,pH=10 时R的平均降解速率为0.04 mol?L-1?min-1 |
| C、溶液酸性越强,R 的降解速率越小 |
| D、R的起始浓度和溶液的PH均影响R的降解速率 |
考点:物质的量或浓度随时间的变化曲线
专题:化学平衡专题
分析:A、根据图中的信息可以知道在0-50min之间,pH=2和pH=7时R的降解百分率;
B、根据平均降解速率v=
来计算即可;
C、对比溶液的酸性强弱对R的降解速率的影响情况;
D、根据题中给出的曲线判断.
B、根据平均降解速率v=
| △c |
| △t |
C、对比溶液的酸性强弱对R的降解速率的影响情况;
D、根据题中给出的曲线判断.
解答:
解:A、根据图示可知:在0-50min之间,pH=2和pH=7时R的降解百分率是相等的,故A错误;
B、在 20-25min之间,pH=10时R的平均降解速率为
×10-4=0.04×10-4mol?L-1?min-1,故B错误;
C、溶液酸性越强,即pH越小,线的斜率越大,可以知道R的降解速率越大,故C错误;
D、根据图中曲线可知,曲线的斜率表示反应速率,起始浓度不同分解速率不同,PH不同分解速率也不同,故R的起始浓度和溶液的PH均影响R的降解速率,故D正确;
故选D.
B、在 20-25min之间,pH=10时R的平均降解速率为
| 0.6-0.4 |
| 5 |
C、溶液酸性越强,即pH越小,线的斜率越大,可以知道R的降解速率越大,故C错误;
D、根据图中曲线可知,曲线的斜率表示反应速率,起始浓度不同分解速率不同,PH不同分解速率也不同,故R的起始浓度和溶液的PH均影响R的降解速率,故D正确;
故选D.
点评:本题考查学生的识图能力,要求学生具有分析和解决问题的能力,难度不大.

练习册系列答案
相关题目
某粒子结构示意图为 ,若该粒子为离子,则它所带的电荷数可能为( )
,若该粒子为离子,则它所带的电荷数可能为( )
①8-n ②n-8 ③10-n ④n-10.
 ,若该粒子为离子,则它所带的电荷数可能为( )
,若该粒子为离子,则它所带的电荷数可能为( )①8-n ②n-8 ③10-n ④n-10.
| A、①② | B、①③ | C、③④ | D、②④ |
下列物质在一定条件下,不能和氢气发生加成反应的是( )
| A、乙醛 | B、丙酮 | C、乙酸 | D、甲苯 |
向含有下列离子的溶液中分别加入烧碱固体(溶液体积变化可忽略),能引起离子浓度减小的是( )
| A、CO32- |
| B、Cl- |
| C、OH- |
| D、Cu2+ |
下列关于乙烯和聚乙烯的叙述不正确的是( )
| A、乙烯常温下是气体,为纯净物;聚乙烯常温下是固体,为混合物 |
| B、乙烯的化学性质比聚乙烯活泼 |
| C、取等质量的乙烯和聚乙烯完全燃烧后,生成的CO2和H2O的质量分别相等 |
| D、乙烯和聚乙烯都能使酸性高锰酸钾溶液褪色 |
关于离子键和离子化合物的说法中,正确的是( )
| A、阴阳离子之间通过静电吸引形成离子键 |
| B、阴阳离子之间通过离子键一定能形成离子化合物 |
| C、离子化合物一定能导电 |
| D、只有在活泼金属元素与活泼非金属元素化合时,才能形成离子键 |
某酸溶液的PH为2,某碱溶液的PH为12,两者等体积相混合后,有关PH值的变化正确的是( )
| A、大于7 | B、小于7 |
| C、等于7 | D、三种都有可能 |