题目内容
【12分】向100 mL 3 mol·L-1硫酸铝铵溶液中逐滴加入1 mol·L-1 Ba(OH)2溶液。
(1)写出刚好出现沉淀的总物质的量为最大值时的离子方程式(用一个式子表示):__________。
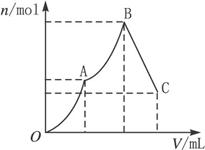
(2)随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如下图所示。
写出B点和C点对应的Ba(OH)2溶液体积:B. _______________,C._______________。
(1)写出刚好出现沉淀的总物质的量为最大值时的离子方程式(用一个式子表示):__________。
(2)随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如下图所示。
写出B点和C点对应的Ba(OH)2溶液体积:B. _______________,C._______________。

(1)Al3++2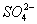 +
+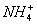 +2Ba2++4 OH-====Al(OH)3↓+2BaSO4↓+NH3·H2O
+2Ba2++4 OH-====Al(OH)3↓+2BaSO4↓+NH3·H2O
(2)600 mL 750 mL
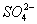 +
+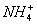 +2Ba2++4 OH-====Al(OH)3↓+2BaSO4↓+NH3·H2O
+2Ba2++4 OH-====Al(OH)3↓+2BaSO4↓+NH3·H2O(2)600 mL 750 mL
(1)解答本题,首先弄清楚明矾、硫酸铝铵与Ba(OH)2溶液反应的区别:K+与OH-不反应,而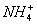 与OH-反应。从图示可看出,在A、B、C三点时反应分别为:
与OH-反应。从图示可看出,在A、B、C三点时反应分别为:
A:2NH4Al(SO4)2+3Ba(OH)2====3BaSO4↓+2Al(OH)3↓+(NH4)2SO4
B:NH4Al(SO4)2+2Ba(OH)2====2BaSO4↓+Al(OH)3↓+NH3·H2O
C:2NH4Al(SO4)2+5Ba(OH)2====4BaSO4↓+Ba(AlO2)2+NH3·H2O
在B点时沉淀的物质的量最大。
(2)在B点时根据反应
n〔Ba(OH)2〕=2n〔NH4Al(SO4)2〕="2×0.1" L×3 mol·L-1="0.6" mol,
故V〔Ba(OH)2〕="0.6" mol÷1 mol·L-1="0.6" L。
在C点时根据反应
n〔Ba(OH)2〕=2.5n〔NH4Al(SO4)2〕="2.5×0.1" L×3 mol·L-1="0.75" mol,
故V〔Ba(OH)2〕="0.75" mol÷1 mol·L-1="0.75" L。
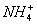 与OH-反应。从图示可看出,在A、B、C三点时反应分别为:
与OH-反应。从图示可看出,在A、B、C三点时反应分别为: A:2NH4Al(SO4)2+3Ba(OH)2====3BaSO4↓+2Al(OH)3↓+(NH4)2SO4
B:NH4Al(SO4)2+2Ba(OH)2====2BaSO4↓+Al(OH)3↓+NH3·H2O
C:2NH4Al(SO4)2+5Ba(OH)2====4BaSO4↓+Ba(AlO2)2+NH3·H2O
在B点时沉淀的物质的量最大。
(2)在B点时根据反应
n〔Ba(OH)2〕=2n〔NH4Al(SO4)2〕="2×0.1" L×3 mol·L-1="0.6" mol,
故V〔Ba(OH)2〕="0.6" mol÷1 mol·L-1="0.6" L。
在C点时根据反应
n〔Ba(OH)2〕=2.5n〔NH4Al(SO4)2〕="2.5×0.1" L×3 mol·L-1="0.75" mol,
故V〔Ba(OH)2〕="0.75" mol÷1 mol·L-1="0.75" L。

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目