题目内容
11.能正确表示下列反应的离子方程式的是( )| A. | 醋酸钠的水解反应:CH3COO-+H2O═CH3COOH+H2O | |
| B. | 碳酸氢钙与过量的NaOH溶液反应:Ca2-+2HCO3-+2OH-═CaCO3↓+2H2O+CO32- | |
| C. | AgNO3溶液中加入过量的氨水:Ag++NH3•H2O═AgOH↓+NH4+ | |
| D. | 稀硝酸与过量的铁屑反应:3Fe+8H++2NO3-═3Fe3++2NO↑+4H2O |
分析 A.醋酸钠水解生成醋酸与氢氧化钠;
B.碳酸氢钙与过量的NaOH溶液反应生成碳酸钙、碳酸钠和水;
C.AgNO3溶液中加入过量的氨水生成银氨溶液;
D.铁过量反应生成二价铁离子.
解答 解:A.醋酸钠水解生成醋酸与氢氧化钠,离子方程式:CH3COO-+H2O?CH3COOH+OH-,故A错误;
B.碳酸氢钙与过量的NaOH溶液反应生成碳酸钙、碳酸钠和水,离子方程式:Ca2-+2HCO3-+2OH-═CaCO3↓+2H2O+CO32-,故B正确;
C.AgNO3溶液中加入过量氨水反应的离子方程式为:Ag++3NH3H2O═Ag(NH3)2++OH-+2H2O+NH4+,故C错误;
D.稀硝酸与过量的铁屑反应,离子方程式:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O,故D错误;
故选:B.
点评 本题考查了离子方程式的书写,明确反应实质及离子方程式的书写是解题关键,题目难度不大,注意银氨溶液的配置.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
19.下列各组离子能在pH=1的无色溶液中大量共存的是( )
| A. | Ba2+、Na+、I-、ClO- | B. | Mg2+、Cl-、CH3COO-、CO32- | ||
| C. | K+、Cl-、Fe2+、NO3- | D. | Ca2+、Cl-、Na+、Br- |
19.电动车电池是一种锂离子电池.根据锂离子电池所用电解质材料不同,锂离子电池可以分为液态锂离子电池(简称为LIB)和聚合物锂离子电池(简称为LIP)两大类,聚合物锂离子电池总反应:LiCoO2+6C$?_{放电}^{充电}$Li1-xCoO2+LixC6,以下说法正确的是( )
| A. | 充电时,阴极反应式:LiCo2-xe-═Li1-xCoO2+xLi+ | |
| B. | 充电时,阳极反应式:6C+xLi++xe-═LixC6 | |
| C. | 充电时,电池的负极与电源的负极相连 | |
| D. | 放电时,Li+向负极移动 |
6.下列物质属于纯净物的是( )
| A. | 聚乙烯 | B. | 冰醋酸 | C. | 福尔马林 | D. | 碘酒 |
20.下列依据相关实验得出的结论正确的是( )
| A. | 向浓度均为0.1 mol•L-1NaCl和NaI混合溶液中滴加少量AgNO3溶液,产生黄色沉淀,说明Ksp(AgCl)>Ksp(AgI) | |
| B. | 在含FeCl2杂质的FeCl3溶液中通足量Cl2后,充分加热,除去过量的Cl2,即可得到较纯净的FeCl3溶液 | |
| C. | 用激光笔分别照射蛋清溶液和葡萄糖溶液,能产生光亮“通路”的是蛋清溶液 | |
| D. | 用铂丝蘸取某溶液进行焰色反应,透过蓝色钴玻璃观察到火焰呈紫色,该溶液一定是钾盐溶液 |
1.下列实验操作或方法中,合理的是( )
| A. | 用铂丝蘸取某溶液置于酒精灯火焰上灼烧,直接观察火焰颜色,检验K+的存在 | |
| B. | 用玻璃棒蘸取Na2CO3溶液,滴在湿润的pH试纸上,测定该溶液的pH | |
| C. | 浓硫酸不慎沾到皮肤上,立即用大量的NaOH溶液冲洗 | |
| D. | 试管可用酒精灯直接加热,也可用水浴加热 |
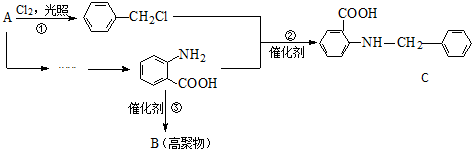
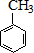 $→_{水浴加热}^{浓H_{2}SO_{4}/浓HNO_{3}}$
$→_{水浴加热}^{浓H_{2}SO_{4}/浓HNO_{3}}$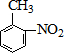
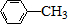 $\stackrel{KMnO_{4}/H+}{→}$
$\stackrel{KMnO_{4}/H+}{→}$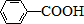
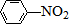 $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$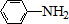 (弱碱性,易被氧化)
(弱碱性,易被氧化) .
.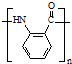 .
.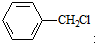 水解产物的同分异构体,且遇氯化铁溶液发生显色反应,X有3种结构.
水解产物的同分异构体,且遇氯化铁溶液发生显色反应,X有3种结构.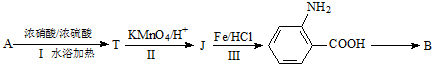
 .
.
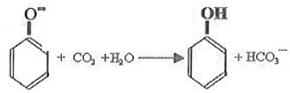

 ;
; .
.