题目内容
【题目】由乙烯和其他无机原料合成环状酯E和高分子化合物H的示意图如下所示:
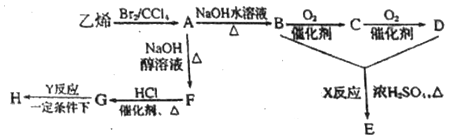
请回答下列问题:
(1)写出以下物质的结构简式:A____________,H_____________,C的化学名称_____________。
(2)写出以下反应的反应类型:X_____________,Y_______________。
(3)写出以下反应的化学方程式:
A→B:___________________________________________;
G→H:_________________________________。
B+D→E:________________________________________。
【答案】 ![]()
![]() 乙二醛 取代反应 加聚反应
乙二醛 取代反应 加聚反应 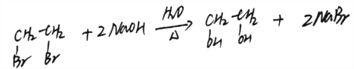
![]()

【解析】乙烯和溴发生加成反应生成A,A的结构简式为:![]() ,A和氢氧化钠的水溶液发生取代反应生成B,B的结构简式为:
,A和氢氧化钠的水溶液发生取代反应生成B,B的结构简式为:![]() ,B被氧气氧化生成C,C的结构简式为:OHC-CHO,C被氧气氧化生成D,D的结构简式为:HOOC-COOH,B和D发生酯化反应生成E,E是环状酯,则E乙二酸乙二酯; A和氢氧化钠的醇溶液发生消去反应生成F,F的结构简式为:
,B被氧气氧化生成C,C的结构简式为:OHC-CHO,C被氧气氧化生成D,D的结构简式为:HOOC-COOH,B和D发生酯化反应生成E,E是环状酯,则E乙二酸乙二酯; A和氢氧化钠的醇溶液发生消去反应生成F,F的结构简式为:![]() ,F和氯化氢发生加成反应生成G氯乙烯,氯乙烯发生加聚反应生成H,H为聚氯乙烯。
,F和氯化氢发生加成反应生成G氯乙烯,氯乙烯发生加聚反应生成H,H为聚氯乙烯。
(1) 通过以上分析知,结构简式A为![]() ,H为
,H为![]() ;C的化学名称为乙二醛;正确答案:
;C的化学名称为乙二醛;正确答案: ![]() ;
; ![]() ; 乙二醛 。
; 乙二醛 。
(2)乙二醇和乙二酸在浓硫酸作用下加热反应生成生成乙二酸乙二酯,,该反应为取代反应;氯乙烯在一定条件下发生加聚反应生成高分子,该反应为加聚反应;正确答案:取代反应;加聚反应。
(3)A→B:1,2-二溴乙烷在氢氧化钠溶液加热的条件下发生取代反应生成乙二醇和溴化钠,反应方程式: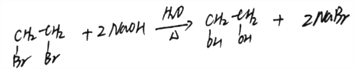 ;正确答案:
;正确答案: 。
。
G→H:一定条件下,氯乙烯发生加聚反应生成聚氯乙烯,反应方程式为![]() ;正确答案:
;正确答案:![]() 。
。
B+D→E:乙二酸和乙二醇在浓硫酸加热条件下发生酯化反应生成乙二酸乙二酯,反应的方程式: ;正确答案:
;正确答案: 。
。

 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案【题目】根据下列实验操作和现象所得出的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向苯酚浊液中滴加Na2CO3溶液,浊液变清 | 苯酚的酸性强于H2CO3的酸性 |
B | 向碘水中加入等体积CCl4,振荡后静置,上层接近无色,下层显紫红色 | I2在CCl4中的溶解度大于在水中的溶解度 |
C | 向CuSO4溶液中加入铁粉,有红色固体析出 | Fe2+的氧化性强于Cu2+的氧化性 |
D | 向NaCl、NaI的混合稀溶液中滴入少量稀AgNO3溶液,有黄色沉淀生成 | Ksp(AgCl) >Ksp(AgI) |
A. A B. B C. C D. D