题目内容
27.铝和氢氧化钾都是重要的工业产品。请回答:(1)工业冶炼铝的化学方程式是___________________________________。
(2)铝与氢氧化钾溶液反应的离子方程式是__________________________________。
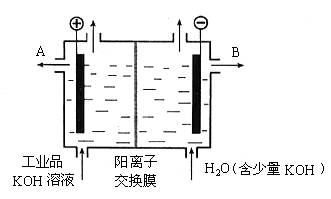
(3)工业品氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。

①该电解槽的阳极反应式是__________________________。
②通电开始后,阴极附近溶液pH会增大,请简述原因
_______________________________________________________。
③除去杂质后的氢氧化钾溶液从液体出口______(填写“A”或“B”)导出。
(1)2Al2O3![]() 4Al+3O2↑
4Al+3O2↑
(2)2Al+2OH-+2H2O=![]() +3H2↑
+3H2↑
(3)①4OH--4e-=2H2O+O2↑
②H+放电,促进水的电离,OH-浓度增大
③B
解析:离子交换膜法电解提纯KOH时,阳极反应为:4OH--4e-=2H2O+O2↑,阴极反应为:4H2O+4e-=4OH-+2H2↑。电解过程中阳极附近的K+通过阳离子交换膜向阴极移动,含氧酸根离子不能通过离子交换膜。一段时间后,阴极附近K+、OH-浓度变大,从B处(阴极区)得到溶液蒸发结晶后可得较纯净的KOH。

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目