题目内容
(7分).短周期元素X和Y属于同一主族。负二价的元素X和氢的化合物在通常状况下是一种液体,其中X的质量分数为88.9%;元素X和元素Y可以形成两种化合物,在这两种化合物中,X的质量分数分别为50%和60%。
(1)确定Y元素在周期表中的位置________________________________。
(2)写出X的质量分数为60%的化合物的化学式__________;该分子中中心原子以sp2杂化,是________分子,分子构型________。
(3)由元素氢、X、Y三种元素形成的化合物常见的有两种,其水溶液均呈酸性,试分别写出其分子式________、________,并比较酸性强弱:________________。
(1)确定Y元素在周期表中的位置________________________________。
(2)写出X的质量分数为60%的化合物的化学式__________;该分子中中心原子以sp2杂化,是________分子,分子构型________。
(3)由元素氢、X、Y三种元素形成的化合物常见的有两种,其水溶液均呈酸性,试分别写出其分子式________、________,并比较酸性强弱:________________。
(1)Y:第3周期、ⅥA族。(2) SO3 非极性 平面三角形 。
(3)H2SO3 H2SO4 H2SO4>H2SO3。
(3)H2SO3 H2SO4 H2SO4>H2SO3。
(1)负二价的元素X和氢的化合物在通常状况下是一种液体,所以X是氧元素,则Y是硫元素,硫位于周期表的第三周期第ⅣA。
(2)硫可以形成SO2和SO3,前者氧元素的含量是50%,后者是60%。三氧化硫者中心原子硫原子没有孤对电子,所以是平面正三角形结构,属于sp2杂化。
(3)H、O、S形成的显酸性的化合物是H2SO4、H2SO3。由于(OH)mROn中n越大,酸性越强,所以根据化学式可知,酸性强弱是H2SO4>H2SO3。
(2)硫可以形成SO2和SO3,前者氧元素的含量是50%,后者是60%。三氧化硫者中心原子硫原子没有孤对电子,所以是平面正三角形结构,属于sp2杂化。
(3)H、O、S形成的显酸性的化合物是H2SO4、H2SO3。由于(OH)mROn中n越大,酸性越强,所以根据化学式可知,酸性强弱是H2SO4>H2SO3。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
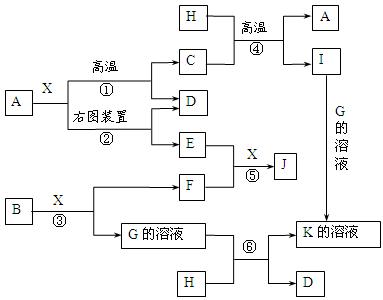
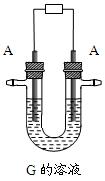
 按要求填空:
按要求填空: 含氯化钠、氯化铁、氯化铜等)进行集中处理,过程如下:
含氯化钠、氯化铁、氯化铜等)进行集中处理,过程如下: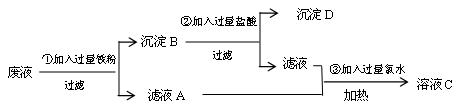
 填“氧化剂”或“还原剂”)。
填“氧化剂”或“还原剂”)。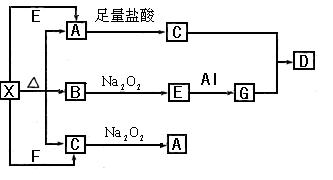
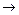 A的离子方程式:_____________________________________
A的离子方程式:_____________________________________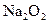 参加反应的化学方程式______________________________________,
参加反应的化学方程式______________________________________,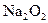 转移的电子数为_____________个。
转移的电子数为_____________个。
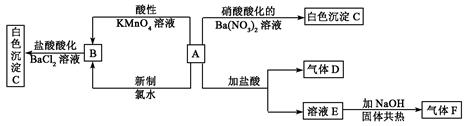
 写出下列物质化学式:A:_________________;C:_________________;
写出下列物质化学式:A:_________________;C:_________________; 离子方程式:
离子方程式: