题目内容
【题目】分枝酸可用于生化研究。其结构简式如图。下列关于分枝酸的叙述正确的是( )

A.可与乙醇、乙酸反应,且反应类型相同
B.分子中含有2种官能团
C.1mol分枝酸最多可与3molNaOH发生中和反应
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
【答案】A
【解析】
A.该物质中含有羧基和羟基,既可以与乙醇发生酯化反应,也可以与乙酸发生酯化反应,反应类型相同,故A正确;
B.该化合物分子中含有羧基、醇羟基、醚键和碳碳双键4种官能团,故B错误;
C.分枝酸中只有羧基能与NaOH溶液发生中和反应,一个分子中含两个羧基,故1mol分枝酸最多能与2mol NaOH发生中和反应,故C错误;
D.该物质使溴的四氯化碳溶液褪色的原理是溴与碳碳双键发生加成反应,而是使酸性高锰酸钾溶液褪色是发生氧化反应,原理不同,故D错误;
故选A。

 优生乐园系列答案
优生乐园系列答案【题目】四氯化锡可用作媒染剂。利用如图所示装置可以制备四氯化锡(部分夹持装置已略去);

有关信息如下表:
化学式 | SnCl2 | SnCl4 |
熔点/℃ | 246 | -33 |
沸点/℃ | 652 | 144 |
其他性质 | 无色晶体,易氧化 | 无色液体,易水解 |
回答下列问题:
(1)戊装置中冷凝管的进水口为___________(填“a”或“b”)。
(2)用甲装置制氯气,MnO4-被还原为Mn2+,该反应的离子方程式为________________________。
(3)将装置如图连接好,检查气密性,慢慢滴入浓盐酸,待观察到___________(填现象)后,开始加热丁装置,锡熔化后适当增大氯气流量,继续加热丁装置,此时继续加热丁装置的目的是:①促进氯气与锡反应;②_______________________________。
(4)如果缺少乙装置,可能产生的后果是___________________;己装置的作用是__________________。
(5)某同学认为丁装置中的反应可能产生SnCl2杂质,以下试剂中可用于检测是否产生SnCl2 的有_______________(填标号)。
a.FeCl3溶液(滴有KSCN) b.H2O2溶液 C.溴水 d.AgNO3溶液
(6)反应中用去锡粒1.19g,反应后在戊装置的试管中收集到2.38 gSnCl4,则SnCl4的产率为____________________。
【题目】A、B、C、D、E是元素周期表中前四周期的五种常见元素,其原子序数依次增大。详细信息见表,请回答下列问题:
① | A的一种核素在考古时常用来鉴定一些文物的年代 |
② | B的氧化物是导致光化学烟雾的主要物质之一 |
③ | C的某一种单质是空气的主要成分之一 |
④ | D的基态原子核外有6个原子轨道处于半充满状态 |
⑤ | E能形成红色的E2O和黑色的EO两种氧化物 |
(1)D的价电子排布式可表示为_______。
(2)BC3-的空间构型为____ (用文字描述)。
(3)根据等电子原理,AC分子的结构式为_____。
(4)1 mol AC2中σ键、π键数目之比为____。
(5)将白色的ESO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配位数是4的配合离子。请写出生成此配合离子的离子方程式:____。
(6)E2+能与NH3、H2O、Cl-等形成配位数为4的配合物。
①[E(NH3)4]2+中存在的化学键类型有____(填序号)。
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
②[E(NH3)4]2+具有对称的空间构型,[E(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[E(NH3)4]2+的空间构型为_____。其中,配体的杂化类型是_____。
(7)E的晶胞如下图所示,E为______堆积,空间利用率为_____,E晶体中每个E原子周围距离最近的E原子数目为____;已知E原子的半径为a nm,阿伏加德罗常数的值为NA,则E晶体的密度是_____g·cm-3。(列出算式即可)。
【题目】TiCl4是制备钛及其化合物的重要中间体,可利用下列装置在实验室制备TiCl4(夹持装置略去): TiO2+2C+2Cl2![]() TiCl4+2CO
TiCl4+2CO
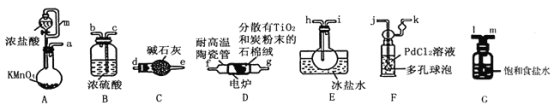
已知:①PdCl2溶液捕获CO时生成Pd单质;②相关数据如下表:
化合物 | 熔点/℃ | 沸点/℃ | 密度/gcm-3 | 溶解性 |
TiCl4 | -25 | 136 | 1.5 | 能溶于有机溶剂:遇水分解生成难溶于水的物质 |
CCl4 | -23 | 76.8 | 1.6 | 难溶于水 |
回答下列问题:
(1)装置A中连通管的作用是______;装置E中使用冰盐水浴的目的是_____________________。
(2)按照气流由左到右的方向,上述装置合理的连接顺序为____________________ (填仪器接口字母);根据完整的实验装置进行实验,实验步骤如下:_____________; 装入药品;向装置A烧瓶中滴加适量浓盐酸,当观察到_________时,加热装置D中陶瓷管;装置E烧瓶中的液体量不再增加时,停止加热,充分冷却。
(3)装置C的作用为___________________。
(4)装置F中发生反应的化学方程式为________________________。
(5)制得的TiCl4中常含有少量CCl4, 从混合液体中分离出TiCl4的操作名称为_______________。
(6)利用如图所示装置测定产品纯度:称取w g TiCl4产品进行实验,向安全漏斗中加入适量蒸馏水,待四氯化钛充分反应后,将烧瓶和安全漏斗中的液体一并转入锥形瓶中,用氢氧化钠溶液调节至中性,滴加几滴0.1 molL-1的K2CrO4溶液作指示剂,用cmol L-1 AgNO3标准溶液滴定至终点( Ag2CrO4为红棕色沉淀,可指示滴定终点),重复滴定两次,平均消耗标准溶液V mL。
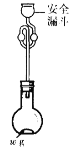
已知:TiCl4 +(2+x)H2O=TiO2xH2O↓+4HCl
①安全漏斗在本实验中的作用除加水外,还有___________。
②根据上述数据计算该产品的纯度为__________。(用含w、c和V的代数式表示)
