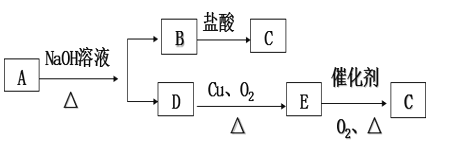
题目内容
【题目】(1)15.6gNa2X中含Na+0.4mol,则Na2X的摩尔质量是____________。
(2)设NA为阿伏加德罗常数的数值,如果a g氧气中含有的分子数为b,则c g氧气在标准状况下的体积约是_________________(用含NA的式子表示)。
(3)某溶液由Mg2+、Al3+、Cl-、SO42- 4种离子组成,测得其中Al3+、SO42-、Cl-的物质的量浓度之比为3:1:13,则溶液中Mg2+、Al3+、SO42-的物质的量浓度之比为___________。
(4)标况下,密度为1.25g/L的CO2与CH4组成的混合气体中,CO2的体积分数为______。
(5)将标准状况下体积为aL的HCl气体溶于1000g水中,得到盐酸的密度为bg/cm3,则该盐酸的物质的量浓度为______________mol/L。
(6)下列各项与胶体性质无关的有______________________。
①卤水点豆腐 ②明矾净水 ③静电除尘 ④油水分离 ⑤血液透析 ⑥三角洲形成 ⑦酸碱中和 ⑧雨后彩虹和海市蜃楼 ⑨臭氧消毒
【答案】78g/mol ![]() 3:3:1 42.86%
3:3:1 42.86% ![]() ④⑦⑨
④⑦⑨
【解析】
(1)先算出Na2X的物质的量,再算其摩尔质量;
(2)先求出cg氧气的物质的量,再利用标准状况下的气体摩尔体积求其体积;
(3)利用电荷守恒(溶液的电中性原则)进行求算;
(4)气体的体积分数在数值上等于其物质的量分数;
(5)利用物质的量浓度的定义式直接进行求算;
(6)胶体的知识主要有布朗运动,丁达尔现象、电泳、聚沉、渗析等;
(1)据Na2X的化学式知,含Na+0.4mol,则Na2X的物质的量为0.2mol,其质量为15.6g,所以Na2X的摩尔质量![]() ;
;
(2) ag氧气中含有的分子数为b,其物质的量为![]() mol,所以cg氧气的物质的量为
mol,所以cg氧气的物质的量为![]() ,其在标准状况下的体积为
,其在标准状况下的体积为![]() =
=![]() ;
;
(3) 在任何一种溶液中,阳离子所带的正电荷总数等于阴离子所带的负电荷总数。在该溶液中则有:c(Mg2+)×2+c(Al3+)×3=c(SO42-)×2+c(Cl-)×1。设Mg2+、Al3+、Cl-、SO42-的物质的量浓度分别为x、3a、13a、a,所以有2x+3×3a=a×2+13a,解得x=3a,所以溶液中c(Mg2+):c(Al3+):c(SO42-)=3a:3a:a=3:3:1;
(4) 设CO2和CH4的物质的量分别为n(CO2)、n(CH4)。CO2的体积分数等于物质的量分数即![]() =
=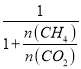 ,所以只需要求出
,所以只需要求出![]() 即可。据密度的本义有:
即可。据密度的本义有: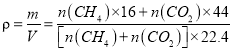 =1.25,求得
=1.25,求得![]() =
=![]() ,所以CO2的体积分数为
,所以CO2的体积分数为![]() =
=![]() ≈42.86%;
≈42.86%;
(5) 该HCl的物质的量为![]() mol,形成溶液的体积为
mol,形成溶液的体积为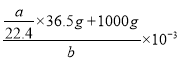 L,所以该盐酸的物质的量浓度c(HCl)=
L,所以该盐酸的物质的量浓度c(HCl)=![]() =
=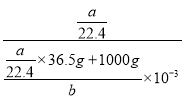 =
=![]() mol/L;
mol/L;
(6)①涉及的是胶体聚沉;②涉及的是胶体的聚沉;③涉及的是胶体的电泳;④涉及的是乳浊液的分离,与胶体无关;⑤涉及的是胶体的渗析;⑥涉及的是胶体的聚沉;⑦涉及的是中和反应,与胶体的性质无关;⑧均与水雾形成的胶体有关,涉及丁达尔现象;⑨臭氧消毒是利用了臭氧的氧化性,与胶体的性质无关;所以答案选择④、⑦、⑨。

 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案【题目】氯化亚砜(SOCl2)常用于医药、农药、染料工业,也可在有机合成工业中作氯化剂。已知:SOCl2的相关性质如下表所示:
颜色、状态 | 熔点 | 沸点 | 腐蚀性 | 水解 |
无色或微黄液体 | -105℃ | 78℃ | 强 | 极易水解 |
现利用如图装置制备SOCl2。

请回答下列问题:
Ⅰ.制备SO2和Cl2。
(1)本实验选用装置甲制备SO2和Cl2,装置甲中仪器x的名称为___;若以KMnO4和浓盐酸反应制备Cl2,反应的离子方程式为___。
Ⅱ.制备SOCl2。
以活性炭作为催化剂,SO2和C12可以和S粉在180~200℃时反应合成SOCl2,选用装置A、B、C、D进行制备(夹持、加热装置略去)。
(2)按气流从左到右的方向,装置A、B、C、D的连接顺序为___(填仪器接口的字母编号)。
(3)试剂y为___(填选项字母,下同);试剂z为___。
A.热水 B.乙醇 C.石蜡油 D.冰水
(4)装置A中U形管内发生反应的化学方程式为___。
(5)装置C的作用为___;若装置A处通入的SO2和Cl2的物质的量之比为1:3,则装置C中生成的盐为___(填化学式);请设计实验验证装置C中生成的盐中含有SO42-:____。