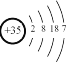题目内容
【题目】元素周期表与元素周期律在学习、研究中有很重要的作用。下表是元素周期表中5种元素的相关信息,其中Q、W、X位于同一周期。
元素 | 信息 |
Q | 地壳中含量第2的元素 |
W | 最高正化合价为+7价 |
X | 最高价氧化物对应的水化物在本周期中碱性最强 |
Y | 焰色反应为紫色 |
Z | 原子结构示意图为 |
(1)Q在元素周期表中的位置是___________。
(2)Q、W的最高价氧化物对应的水化物中,酸性较强的物质是___________。(填化学式)
(3)金属性Y强于X,用原子结构解释原因:___________,失电子能力Y大于X。(用元素符号回答问题)
(4)下列对于Z及其化合物的推断中,正确的是___________(填序号)。
①Z的最低负化合价与W的最低负化合价相同
②Z的氢化物的稳定性弱于W的氢化物的稳定性
③Z的单质可与X和W形成的化合物的水溶液发生置换反应
【答案】第3周期、第ⅣA族 HClO4 同主族电子层增多,失电子能力增强 ①②
【解析】
Q是地壳中含量第2的元素,则Q为Si;Q、W、X位于同一周期,均在第三周期,W的最高正化合价为+7价,W为Cl;X的最高价氧化物对应的水化物在本周期中碱性最强,X为Na;Y的焰色反应为紫色,Y为K,Z的原子结构示意图为  ,Z为Br,以此来解答。
,Z为Br,以此来解答。
由分析知:Q为Si、W为Cl、X为Na、Y为K、Z为Br;
(1)Q为Si,核电荷数为14,其在元素周期表中的位置是第3周期、第ⅣA族;
(2)非金属性越强,对应最高价含氧酸的酸性越强,Cl的非金属性比Si强,则Si、Cl的最高价氧化物对应的水化物中,酸较强的物质是HClO4;
(3)金属性Y强于X,用原子结构解释原因:K、Na同属于一个主族,且钾的电子层数大于钠的电子层数,原子半径越大,失电子能力增强,所以失去电子能力K大于Na;
(4)①Cl和Br为同主族元素,最低负化合价均为-1价,故①正确;
②非金属性Cl>Br,则HBr的氢化物的稳定性弱于HCl的稳定性,故②正确;
③Br的非金属性小于Cl,则Br2与NaCl溶液不能发生置换反应生成Cl2,故③错误;
故答案为:①②。

【题目】在2L密闭容器中充入气体A和B,发生A(g)+B(g)C(g)+2D(g) ΔH,所得实验数据如表。下列说法不正确的是
实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
n(A) | n(B) | n(C) | ||
① | 300 | 0.40 | 0.10 | 0.090 |
② | 500 | 0.40 | 0.10 | 0.080 |
③ | 500 | 0.20 | 0.05 | a |
A.ΔH>0
B.500 ℃该反应的平衡常数K=0.16 mol·L-1
C.③中达到平衡时,A的转化率大于20%
D.5min末测得①中n(C)=0.050 mol,则0到5min内v(D)=0.02mol·L-1·min-1