题目内容
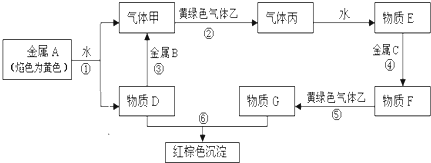
现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下转化关系(图中有些反应的产物和反应的条件没有全部标出).

请根据图中信息回答下列问题:
(1)写出下列物质的化学式:B
(2)写出下列反应离子方程式:
反应①
反应④
(3)反应⑤属于下列反应类型中
A.氧化还原反应 B.分解反应 C.化合反应 D.复分解反应.

请根据图中信息回答下列问题:
(1)写出下列物质的化学式:B
Al
Al
、CFe
Fe
、HFe(OH)3
Fe(OH)3
、丙HCl
HCl
(2)写出下列反应离子方程式:
反应①
2Na+2H2O=2Na++2OH-+H2↑
2Na+2H2O=2Na++2OH-+H2↑
反应④
Fe+2H+=Fe2++H2↑
Fe+2H+=Fe2++H2↑
(3)反应⑤属于下列反应类型中
AC
AC
(填写序号).A.氧化还原反应 B.分解反应 C.化合反应 D.复分解反应.
分析:金属A焰色反应为黄色,应为Na,与水反应生成D为NaOH,则气体甲为H2,B能与NaOH溶液反应生成氢气,应为Al,黄绿色气体乙为Cl2,气体丙为HCl,E为盐酸,红褐色沉淀为Fe(OH)3,G为FeCl3,则C为Fe,F为FeCl2,结合对应物质的性质以及题目要求可解答该题.
解答:解:金属A焰色反应为黄色,应为Na,与水反应生成D为NaOH,则气体甲为H2,B能与NaOH溶液反应生成氢气,应为Al,黄绿色气体乙为Cl2,气体丙为HCl,E为盐酸,红褐色沉淀为Fe(OH)3,G为FeCl3,则C为Fe,F为FeCl2,
(1)由以上分析可知B为Al,C为Fe,H为Fe(OH)3,丙为HCl,故答案为:Al;Fe;Fe(OH)3;HCl;
(2)反应①为钠与水的反应,反应的离子方程式为2Na+2H2O=2Na++2OH-+H2↑,反应④铁与盐酸的反应,反应的离子方程式为Fe+2H+=Fe2++H2↑,
故答案为:2Na+2H2O=2Na++2OH-+H2↑;Fe+2H+=Fe2++H2↑;
(3)反应⑤为2FeCl2+Cl2=2FeCl3,为氧化还原反应和化合反应,故答案为:AC.
(1)由以上分析可知B为Al,C为Fe,H为Fe(OH)3,丙为HCl,故答案为:Al;Fe;Fe(OH)3;HCl;
(2)反应①为钠与水的反应,反应的离子方程式为2Na+2H2O=2Na++2OH-+H2↑,反应④铁与盐酸的反应,反应的离子方程式为Fe+2H+=Fe2++H2↑,
故答案为:2Na+2H2O=2Na++2OH-+H2↑;Fe+2H+=Fe2++H2↑;
(3)反应⑤为2FeCl2+Cl2=2FeCl3,为氧化还原反应和化合反应,故答案为:AC.
点评:本题考查无机物的推断,题目难度中等,注意根据物质的颜色作为推断的突破口,把握物质的转化关系,牢固掌握相关物质的性质为解答该题关键.

练习册系列答案
相关题目