��Ŀ����
����Ŀ�������й��Ȼ�ѧ����ʽ��������ȷ�ĺ��ƣ� ��
A.��֪2H2O��l���T2H2��g��+O2��g����H=+571.6KJmol��1 �� ����H2��ȼ����
B.��֪C��ʯī��s��=C�����ʯ��s����H��0�����Ƚ϶��ߵ��ȶ���
C.��֪500�桢30MPa�£���0.5molN2��1.5molH2�����ܱյ������г�ַ�Ӧ����NH3��g�����ų�19.3KJ�����������Ƴ��÷�Ӧ���Ȼ�ѧ����ʽ
D.��֪2C��s��+2O2��g���T2CO2��g����H1��2C��s��+O2��g���T2CO��g����H2 �� ���ó���H2����H1
���𰸡�C
���������⣺A����֪2H2O��l���T2H2��g��+O2��g����H=+571.6KJmol��1 �� ��2H2��g��+O2��g��=2H2O��l����H=��571.6kJ/mol��������ȼ����Ϊ ![]() =285.8kJ/mol����A����
=285.8kJ/mol����A����
B����֪C��ʯī��s��=C�����ʯ��s����H��0���÷�ӦΪ���ȷ�Ӧ��˵��ʯī���е�����С�ڽ��ʯ����ʯī���ȶ��Դ��ڽ��ʯ����B����
C����֪500�桢30MPa�£���0.5molN2��1.5molH2�����ܱյ������г�ַ�Ӧ����NH3��g�����ų�19.3KJ�����������ڸ÷�ӦΪ���淴Ӧ����������÷�Ӧ�����ɰ��������ʵ����������Ƴ��÷�Ӧ���Ȼ�ѧ����ʽ����C��ȷ��
D����Ӧ2C��s��+2O2��g���T2CO2��g����H1��2C��s��+O2��g���T2CO��g����H2�У�ǰ����ȫȼ�գ����߲���ȫȼ�գ�����߷ų������϶࣬����ʱ�Ϊ��ֵ��֪��H2����H1 �� ��D����
��ѡC��

 Сѧ�����ҵ���ϴ�ѧ������ϵ�д�
Сѧ�����ҵ���ϴ�ѧ������ϵ�д� ���Ž�����ٰθ��νӹ㶫���������ϵ�д�
���Ž�����ٰθ��νӹ㶫���������ϵ�д� �����������ҵ�������������ϵ�д�
�����������ҵ�������������ϵ�д� ѧ���������ν��Ͼ���ѧ������ϵ�д�
ѧ���������ν��Ͼ���ѧ������ϵ�д�����Ŀ������ͭ���ʼ��仯����Ӧ�÷�Χ�ܹ㣮���к��Ȼ��������ʵ��Ȼ�ͭ���壨CuCl22H20����Ϊ��ȡ������CuCl22H20�����Ƚ����Ƴ�ˮ��Һ��Ȼ����ͼ��������ᴿ�� 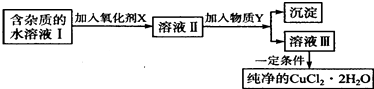
��֪Cu2+��Fe3+��Fe2+���������↑ʼ�����ͳ�����ȫʱ��pH��������
Fe3+ | Fe2+ | Cu2+ | |
�������↑ʼ����ʱ��PH | 1.9 | 7.0 | 4.7 |
����������ȫ����ʱ��PH | 3.2 | 9.0 | 6.7 |
��ش��������⣮
��1�����ʺ���������X���� ��
A.K2Cr207
B.NaCl0
C.H202
D.KMn04
��2�����������Y�� ��
A.CuO
B.NaOH
C.Cu2��OH��2CO3
D.NH3
��3������Һ����CuCl22H2O����Ҫ�����������˲�����
��4���ⶨ��Һ����Fe2+��Ũ�ȣ�����KMnO4����Һ�ζ���ȡ��KMnO4��ҺӦʹ��������ʽ����ʽ�����ζ��ܣ���Ӧ�Ļ�ѧ����ʽ�� ��
����Ŀ������ͭ���ʼ��仯����Ӧ�÷�Χ�ܹ㣮���к��Ȼ��������ʵ��Ȼ�ͭ���壨CuCl22H20����Ϊ��ȡ������CuCl22H20�����Ƚ����Ƴ�ˮ��Һ��Ȼ����ͼ��������ᴿ�� 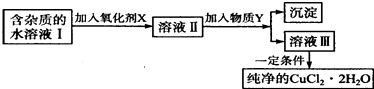
��֪Cu2+��Fe3+��Fe2+���������↑ʼ�����ͳ�����ȫʱ��pH��������
Fe3+ | Fe2+ | Cu2+ | |
�������↑ʼ����ʱ��PH | 1.9 | 7.0 | 4.7 |
����������ȫ����ʱ��PH | 3.2 | 9.0 | 6.7 |
��ش��������⣮
��1�����ʺ���������X���� ��
A.K2Cr207
B.NaCl0
C.H202
D.KMn04
��2�����������Y�� ��
A.CuO
B.NaOH
C.Cu2��OH��2CO3
D.NH3
��3������Һ����CuCl22H2O����Ҫ�����������˲�����
��4���ⶨ��Һ����Fe2+��Ũ�ȣ�����KMnO4����Һ�ζ���ȡ��KMnO4��ҺӦʹ��������ʽ����ʽ�����ζ��ܣ���Ӧ�Ļ�ѧ����ʽ�� ��