题目内容
【题目】A、B、C、D四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和。
(1)A为___,B为_____,C为______,D的最高价氧化物的水化物是_______。
(2)A、B两元素形成化合物属_________(“离子”或“共价”)化合物。写出AB2和E反应的化学方程式:_________________________。
(3)写出D的最高价氧化物的水化物和A反应的化学方程式,并用单线桥标出电子转移的方向和数目__________。
【答案】 C(碳) O(氧) Na(钠) H2SO4 共价 2Na2O2+2CO2=2Na2CO3+O2 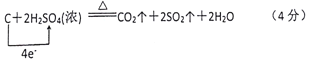
【解析】A、B、C、D四种元素,原子序数依次增大,B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,可知E为过氧化钠,B元素为O元素,C元素为Na元素;A原子的最外层上有4个电子,处于ⅣA族,原子序数小于氧,故A为碳元素;D的L层电子数等于K、M两个电子层上的电子数之和,则M层电子数为8-2=6,故D为S元素。则
(1)由上述分析可知,A为C元素,B为O元素,C为Na。D为S元素,其最高价氧化物的水化物是H2SO4;
(2)A、B两元素形成化合物有CO、CO2,属于共价化合物;CO2能与E(即过氧化钠)反应,化学方程式为:2CO2+2Na2O2=2Na2CO3+O2;(3)D的最高价氧化物的水化物浓硫酸具有强氧化性,和C发生氧化还原反应生成CO2、SO2和H2O,反应的化学方程式为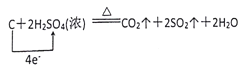 。
。

 名校课堂系列答案
名校课堂系列答案【题目】
1、某学生用0.1 mol·L-1的KOH标准溶液滴定未知浓度的盐酸,其操作分解为如下几步:
A.移取20mL待测盐酸注入洁净的锥形瓶中,并加入2~3滴酚酞; |
B.用标准溶液润洗滴定管2~3次; |
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液; |
D.取标准KOH溶液注入碱式滴定管至刻度“0”以上1~2cm 处; |
E.调节液面至“0”或“0”以下刻度,记下读数;
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度.
就此实验完成填空:
(1)正确操作步骤的顺序是(用序号字母填写)__________AF。
(2)上述B步骤操作的目的是_____________。
(3)在进行C步操作滴定前排气泡时,应选择下图2中的 (填序号),若用25mL滴定管进行实验,当滴定管中的液面在“10”处,则管内液体的体积(填序号)____________(①=10mL,②=15mL,③<10mL,④>15mL)。

(4)判断以下操作,对测定结果盐酸浓度的影响(填“偏高”、“偏低”或““无 影响”)
①上述A步骤操作之前,若先用待测溶液润洗锥形瓶,则对滴定结果的影响是__________。
②若称取一定量的KOH固体(含少量NaOH)配制标准溶液并用来滴定上述盐酸,则对滴定结果产生的影响是____________。
③如果滴定前装有待测溶液的酸式滴定管尖嘴部分有气泡,而滴定结束后气泡消失,则测定结果将__________。



