题目内容
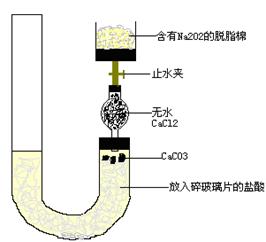
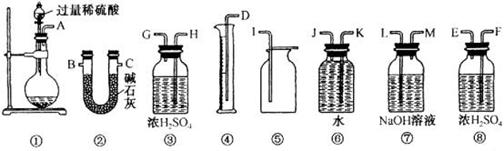
用金属钠制取氧化钠通常采用下法:2NaNO2+6Na=4Na2O+N2↑,试说明为什么用此法制取氧化钠比直接钠氧化法好。
Na2O在N2气中不被氧化,从而分析出Na直接氧化法不足之处;无论金属钠是在氧气中点燃,还是在空气中氧化,因生成的Na2O极不稳定,会进一步氧化生成Na2O2,即2Na+O2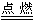 Na2O2,而实际上得不到纯Na2O。
Na2O2,而实际上得不到纯Na2O。
 Na2O2,而实际上得不到纯Na2O。
Na2O2,而实际上得不到纯Na2O。这题属于信息给予题,解答中必须紧扣题干Na2O制取反应式:2NaNO2+6Na=4Na2O+N2↑,反应中生成N2这一重要信息,才可找出答案:Na2O在N2气中不被氧化,从而分析出Na直接氧化法不足之处;无论金属钠是在氧气中点燃,还是在空气中氧化,因生成的Na2O极不稳定,会进一步氧化生成Na2O2,即2Na+O2 Na2O2,而实际上得不到纯Na2O。
Na2O2,而实际上得不到纯Na2O。
 Na2O2,而实际上得不到纯Na2O。
Na2O2,而实际上得不到纯Na2O。
练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
 %,该固体是( )
%,该固体是( )