题目内容
【题目】任意两个环共用两个不直接相连的碳原子的有机化合物称为桥环化合物,二环[1,1,0]丁烷(![]() )是最简单的桥环化合物。下列有关该化合物的叙述不正确的是( )
)是最简单的桥环化合物。下列有关该化合物的叙述不正确的是( )
A.与1,3-丁二烯互为同分异构体
B.其二氯代物有3种(不考虑立体异构)
C.4个碳原子不在同一个平面
D.1mol该物质完全燃烧时最多消耗5.5molO2
【答案】B
【解析】
A.该化合物的分子式为C4H6,与1,3-丁二烯的分子式相同,但结构不同,互为同分异构体,故A不符合题意;
B.当2个Cl取代同一碳原子上的2个H时有![]() 1种,当2个Cl取代不同碳原子上的H时有
1种,当2个Cl取代不同碳原子上的H时有![]() 3种,则其二氯代物有4种,故B符合题意;
3种,则其二氯代物有4种,故B符合题意;
C.该物质分子中存在一个碳原子与其它3个碳原子成单键,成键的4个碳原子不可能共面,故C不符合题意;
D.1molC完全燃烧消耗1molO2,1molH完全燃烧消耗0.25molO2,因此1mol该有机物完全燃烧时最多消耗(4+6×0.25)mol=5.5molO2,故D不符合题意;
故答案为:B。

【题目】硫酸是重要的化工原料,生产过程中SO2催化氧化生成SO3的化学反应为:2SO2(g)+O2(g)![]() 2SO3(g)。
2SO3(g)。
(1)实验测得SO2反应生成SO3的转化率与温度、压强有关,请根据下表信息,结合工业生产实际,选择最合适的生产条件是__。
SO2压强 转化率 温度 | 1个大气压 | 5个大气压 | 10个大气压 | 15个大气压 |
400℃ | 0.9961 | 0.9972 | 0.9984 | 0.9988 |
500℃ | 0.9675 | 0.9767 | 0.9852 | 0.9894 |
600℃ | 0.8520 | 0.8897 | 0.9276 | 0.9468 |
(2)反应2SO2(g)+O2(g)![]() 2SO3(g)达到平衡后,改变下列条件,能使SO2(g)平衡浓度比原来减小的是__(填字母)。
2SO3(g)达到平衡后,改变下列条件,能使SO2(g)平衡浓度比原来减小的是__(填字母)。
A.保持温度和容器体积不变,充入1molO2(g)
B.保持温度和容器体积不变,充入2molSO3(g)
C.降低温度
D.在其他条件不变时,减小容器的容积
(3)某温度下,SO2的平衡转化率(α)与体系总压强(P)的关系如图所示。2.0molSO2和1.0molO2置于10L密闭容器中,反应达平衡后,体系总压强为0.10MPa。平衡状态由A变到B时,平衡常数K(A)__K(B)(填“>”、“<”或“=”),B点的化学平衡常数是__。
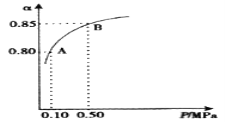
(4)在一个固定容积为5L的密闭容器中充入0.20molSO2和0.10molO2,t1时刻达到平衡,测得容器中含SO30.18mol。
①tl时刻达到平衡后,改变一个条件使化学反应速率发生如图所示的变化,则改变的条件是__。
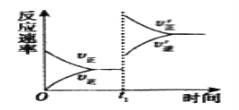
A.体积不变,向容器中通入少量O2
B.体积不变,向容器中通入少量SO2
C.缩小容体积
D.升高温度
E.体积不变,向容器中通入少量氮气
②若继续通入0.20molSO2和0.10molO2,则平衡__移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,_mol<n(SO3)<_mol。