题目内容
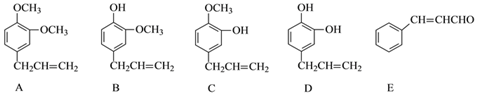
【题目】现有部分短周期元素的性质或原子结构如表所示:
元素编号 | 元素性质或原子结构 |
T | M层上电子数是K层上电子数的3倍 |
X | 最外层电子数是次外电子数的2倍 |
Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
Z | 元素最高正价是+7价 |
(1)元素X位于元素周期表的第________周期______族;
(2)元素Y的原子结构示意图为________。
(3)元素Z与元素T相比,非金属性较强的是________(用元素符号表示),下列表述中能证明这一事实的是________(填序号)。
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
【答案】二 ⅣA 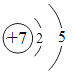 Cl b
Cl b
【解析】
M层上电子数是K层上电子数的3倍,即M层有6个电子,T元素应该是S元素。最外层电子数是次外层电子数的2倍,则X应该是碳元素。常温下单质为双原子分子,其氢化物水溶液呈碱性,因此Y是氮元素。元素最高正价是+7价,则Z是氯元素。据此解答。
根据以上分析可知X是C,Y是N,Z是Cl,T是S。则
(1)碳元素的原子序数是6,则元素X位于元素周期表的第二周期第ⅣA族;
(2)元素Y是氮元素,其原子结构示意图为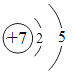 ;
;
(3)同主族自左向右非金属性逐渐增强,则元素Z与元素T相比,非金属性较强的是Cl。
a.常温下Z的单质和T的单质状态不同,非金属性强弱与单质的状态没有关系,a错误;
b. 非金属性越强,氢化物越稳定,Z的氢化物比T的氢化物稳定,说明氯元素的非金属性强于硫元素,b正确;
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应与非金属性强弱没有关系,c错误;
答案选b。

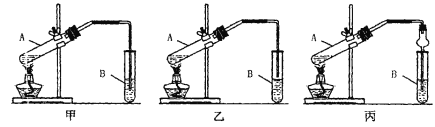
【题目】向如图所示装置中缓慢通入气体X,若打开活塞K,则品红溶液褪色;若关闭活塞K,则品红溶液无变化而澄清石灰水变浑浊。X和Y可能是( )
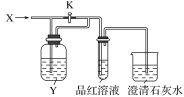
选项 | A | B | C | D |
X | SO2 | Cl2 | HCl | NO2 |
Y | NaOH溶液 | 饱和NaHCO3溶液 | 饱和NaCl溶液 | Na2SO3溶液 |
A. A B. B C. C D. D
【题目】某化学兴趣小组欲测定 KClO3溶液与NaHSO3溶液反应的化学反应速率。所用试剂为10mL0.1mol/LKClO3溶液和10mL0.3mol/LNaHSO3溶液,所得数据如图所示。
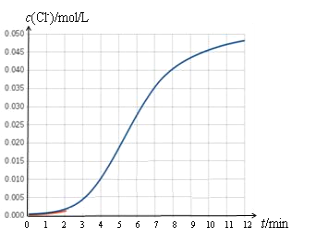
已知:ClO3 + 3HSO3=Cl + 3SO42 + 3H+
(1)根据实验数据可知,该反应在0~4min的平均反应速率:v(Cl-)=_________mol/(L·min)。
(2)某同学仔细分析实验数据后发现,在反应过程中,该反应的化学反应速率先增大后减小。某小组同学针对这一现象进一步通过测定 c(Cl-)随时间变化的曲线探究影响因素,具体如下表所示。
方案 | 假设 | 实验操作 |
I | 该反应放热,使溶液温度升高,反应速率加快 | 向烧杯中加入10mL0.1mol/LKClO3溶液和10mL0.3mol/LNaHSO3溶液, |
II | 取10mL0.1mol/LKClO3溶液加入烧杯中,向其中加入少量NaCl固体,再加入10mL0.3mol/LNaHSO3溶液。 | |
III | 溶液酸性增强加快了化学反应速率 | 分别向2只烧杯中加入10mL0.1mol/LKClO3溶液;向烧杯①中加入1 mL水,向烧杯②中加入1mL0.2mol/L 盐酸;再分别向2只烧杯中加入10mL0.3mol/LNaHSO3溶液。 |
①补全方案I中的实验操作:_____。
②方案II中的假设为_____。
③除I、II、III中的假设外,还可以提出的假设是_____。
④在已知方案 I 的假设不成立的情况下,某同学从控制变量的角度思考,认为方案III中实验操作设计不严谨,请进行改进:_____。
⑤反应后期,化学反应速率变慢的原因是_____。