题目内容
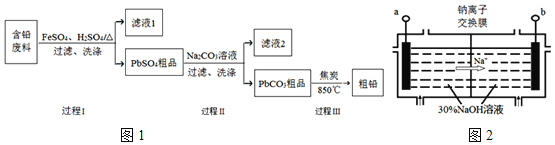
【题目】以废旧铅酸电池中的含铅废料(Pb、PbO、PbO2、PbSO4及炭黑等)为原料,制备粗铅,实现铅的再生利用.其工作流程如图1所示:
已知:Ksp(PbSO4)=1.6×10-5,Ksp(PbCO3)=3.3×10-14.
(1)过程Ⅰ中,在Fe2+催化下,Pb和PbO2反应生成PbSO4的化学方程式是______.
(2)过程Ⅰ中,Fe2+催化过程可表示为:
![]()
![]() .
.
![]() 写出ii的离子方程式:______.
写出ii的离子方程式:______.
![]() 下列实验方案可证实上述催化过程.将实验方案补充完整.
下列实验方案可证实上述催化过程.将实验方案补充完整.
![]() 向酸化的FeSO4溶液中加入KSCN溶液,溶液几乎无色,再加入少量PbO2,溶液变红.
向酸化的FeSO4溶液中加入KSCN溶液,溶液几乎无色,再加入少量PbO2,溶液变红.
![]() ______.
______.
(3)过程Ⅱ的目的是脱硫.若滤液2中c(SO42-)=1.6molL-1,c(CO32-)=0.1molL-1,则PbCO3中______![]() 填“是”或“否”
填“是”或“否”![]() 混有PbSO4.
混有PbSO4.
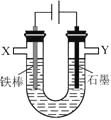
(4)钠离子交换膜固相电解法是从含铅废料中提取铅的一种新工艺,其装置如图2所示.将含铅废料投入阴极室,含铅废料中的PbSO4与NaOH溶液发生反应:![]()
![]() 与外接电源的______极相连.
与外接电源的______极相连.
![]() 电解过程中,PbO2、PbO、HPbO2-在阴极放电,其中PbO2放电的电极反应式为______.
电解过程中,PbO2、PbO、HPbO2-在阴极放电,其中PbO2放电的电极反应式为______.
![]() 与传统无膜固相电解法相比,使用钠离子交换膜可以提高Pb元素的利用率,原因是______.
与传统无膜固相电解法相比,使用钠离子交换膜可以提高Pb元素的利用率,原因是______.
【答案】![]() 4
4![]()
![]()
![]() 取a中红色溶液少量,加入足量Pb,充分反应后,红色褪去 否 负
取a中红色溶液少量,加入足量Pb,充分反应后,红色褪去 否 负 ![]() 阻止HPbO2-进入阳极室被氧化
阻止HPbO2-进入阳极室被氧化
【解析】
(1)在催化下,Pb、PbO2和H2SO4反应生成PbSO4和水,据此书写反应方程式;
(2)①根据题给信息知反应i中Fe2+被PbO2氧化为Fe3+,则反应ii中Fe3+被Pb还原为Fe2+,据此书写离子方程式;
②加入过量的Pb平衡逆向进行充分反应后,红色褪去;
(3)根据Ksp(PbCO3)=3.3×10-14和c(CO32-)=0.1molL-1计算出c(Pb2+)利用浓度积Qc和Ksp(PbSO4)之间的大小关系确定PbCO3中是否混有PbSO4;
(4)①根据钠离子的移动方向确定阴阳极;
②电解过程中,PbO2在阴极得电子,发生还原反应;
③钠离子交换膜只允许钠离子通过。
(1)根据题给化学工艺流程知,过程Ⅰ中,在催化下,Pb、PbO2和H2SO4反应生成PbSO4和水,化学方程式为:![]()
![]()
![]() ;
;
(2)①催化剂通过参加反应,改变反应历程,降低反应的活化能,加快化学反应速率,而本身的质量和化学性质反应前后保持不变,根据题给信息知反应i中Fe2+被PbO2氧化为Fe3+,则反应ii中Fe3+被Pb还原为Fe2+,离子方程式为:![]() ;
;
②a实验证明发生反应i,则b实验需证明发生反应ii,实验方案为:
![]() 向酸化的FeSO4溶液中加入KSCN溶液,溶液几乎无色,再加入少量PbO2,溶液变红,亚铁离子被氧化为铁离子,
向酸化的FeSO4溶液中加入KSCN溶液,溶液几乎无色,再加入少量PbO2,溶液变红,亚铁离子被氧化为铁离子,
![]() 取a中红色溶液少量,溶液中存在平衡,
取a中红色溶液少量,溶液中存在平衡,![]() ,加入过量Pb,和平衡状态下铁离子反应生成亚铁离子,平衡逆向进行充分反应后,红色褪去,
,加入过量Pb,和平衡状态下铁离子反应生成亚铁离子,平衡逆向进行充分反应后,红色褪去,
(3)因为Ksp(PbCO3)=3.3×10-14和c(CO32-)=0.1molL-1,可知c(Pb2+)=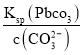 =
=![]() mol/L=3.3×10-13 mol/L , 因此Qc= c(Pb2+) c(SO42-)=3.3×10-13×1.6=5.28×10-13< Ksp(PbSO4),说明PbSO4在母液中未饱和,即PbCO3中不混有PbSO4;
mol/L=3.3×10-13 mol/L , 因此Qc= c(Pb2+) c(SO42-)=3.3×10-13×1.6=5.28×10-13< Ksp(PbSO4),说明PbSO4在母液中未饱和,即PbCO3中不混有PbSO4;
(4)①根据钠离子向阴极移动知,b为阴极,与电源负极相连;
②电解过程中,PbO2在阴极得电子,发生还原反应,电极反应式为![]() ;
;
③钠离子交换膜只允许钠离子通过,阻止HPbO2-进入阳极室被氧化,从而提高Pb元素的利用率;

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案【题目】元素周期表中七个周期可填充的元素种类如下表所示:
周期数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
元素种类 | 2 | 8 | 8 | 18 | 18 | 32 | 32 |
(1)第6、7周期均比第4、5周期多了14种元素,其原因是__。
(2)周期表中__族所含元素最多。
(3)请分析周期数与元素种类的关系,可推测出第8周期可能含有的元素种类为__(填序号)。
A.18 B.32 C.50 D.64
【题目】2020年5月1日起,新版《北京市生活垃圾管理条例》正式实施,下列垃圾分类对应不正确的是
|
|
|
|
A. 鸡蛋壳、剩饭菜 | B. 市民使用后一次性口罩 | C. 过期药品 | D. 一 次性干电池 |
A.AB.BC.CD.D