题目内容
【题目】(1)请按要求填空:用已准确称量的Na2CO3固体配制0.10mol/L Na2CO3溶液100mL,所需要的仪器除烧杯、量筒、玻璃棒和胶头滴管外,还需要的仪器为__________________。
(2)实验室可用下图装置(加热装置略)制取SO2以及验证SO2性质
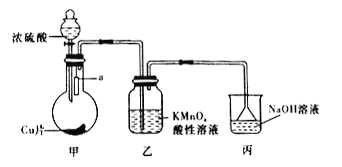
①甲装置中制取SO2气体的化学方程式是___________________________________。
②为了证明SO2具有酸性,a处可放置_________试纸;装置乙中现象为溶液褪色,可证明SO2具有________性。
③ 丙装置的作用是_______________________________。
【答案】 100 mL 容量瓶 Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O 湿润的蓝色石蕊(或pH) 还原 吸收多余的SO2气体、并防止溶液倒吸
CuSO4+SO2↑+2H2O 湿润的蓝色石蕊(或pH) 还原 吸收多余的SO2气体、并防止溶液倒吸
【解析】(1)用已准确称量的Na2CO3固体配制0.10mol/L Na2CO3溶液100mL,所需要的仪器除烧杯、量筒、玻璃棒和胶头滴管外,配制100mL溶液,选100mL容量瓶来配制;
(2)①加热条件下,浓硫酸和铜发生氧化还原反应生成二氧化硫气体,反应的方程式为Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O;
CuSO4+SO2↑+2H2O;
②二氧化硫为酸性气体,可使湿润的蓝色石蕊变红,具有还原性,可与酸性高锰酸钾发生氧化还原反应,可观察到乙溶液褪色;
③二氧化硫有毒,污染环境,可与氢氧化钠反应,可用氢氧化钠溶液吸收,用导致的漏斗可起到防倒吸的作用。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】根据下列实验现象所得出的结论错误的是
选项 | 实验 | 现象 | 结论 |
A | 向KBrO3溶液中加入少量苯,然后通入少量Cl2 | 有机层呈橙色 | 氧化性:Cl2> KBrO3 |
B | 向KNO3和KOH混合溶液中加入铝粉并加热, 将湿润的红色石蕊试纸放在试管口 | 试纸变为蓝色 | NO3-被还原为NH3 |
C | 向0.1 molL-1的Na2CO3溶液中加入两滴酚酞,溶液显浅红色,微热 | 红色加深 | 盐类水解是吸热反应 |
D | 将0. 1 mol L-1的MgSO4溶液滴入到NaOH溶液中至不再有沉淀产生,再滴加0.1 molL-1的CuSO4溶液 | 白色沉淀逐渐变为蓝色沉淀 | Ksp[Cu(OH)2]< Ksp[Mg(OH)2] |
A. A B. B C. C D. D
【题目】二氧化碳被认为是加剧温室效应的主要物质,资源化利用二氧化碳不仅可减少温室气体的排放,还可重新获得燃料或重要工业产品。
Ⅰ.有科学家提出可利用FeO吸收和利用CO2,相关的热化学方程式如下:
6FeO(s)+CO2(g)=2Fe3O4(s)+C(s) , ΔH=-76.0 kJ·mol-1
②3FeO(s)+H2O(g)= Fe3O4(s)+H2(g) ΔH=-18.7 kJ·mol-1
(1)在上述反应中①中,每吸收1molCO2,就有_______molFeO被氧化。
(2)试写出C(s)与水蒸气反应生成CO2和H2的热化学方程式___________。
Ⅱ.一定条件下,二氧化碳转化为甲烷。向一容积为2L的恒容密闭容器中充人一定量的CO2和H2,在300℃时发生上述反应的反应CO2(g)+4H2(g) ![]() CH4(g)+2H2O(g) 。达到平衡时,各物质的浓度分别为CO2 0.2mol·L-1、CH4 0.8mol·L-1、H2 0.8mol·L-1,H2O 1.6mol·L-1。
CH4(g)+2H2O(g) 。达到平衡时,各物质的浓度分别为CO2 0.2mol·L-1、CH4 0.8mol·L-1、H2 0.8mol·L-1,H2O 1.6mol·L-1。
(3)在300℃是,将各物质按下列起始浓度(mol·L-1)加入该反应容器中,达到平衡后,各组分浓度与上述题中描述的平衡浓度相同的是_____________。
选项 | CO | H2 | CH4 | H2O |
A | 0 | 0 | 1 | 2 |
B | 2 | 8 | 0 | 0 |
C | 1 | 4 | 1 | .2 |
D | 0.5 | 2 | 0.5 | 1 |
(4)若保持温度不变,再向该容器内充入与起始量相等的CO2和H2,重新达到平衡时,CH4的浓
度________(填字母)。
A.c(CH4)=0.8mol·L-1 B.0.8mol L-1 >c(CH4) >1.6mol L-1
C.c(CH4)=l.6mol·L-1 D.C(CH4)>1.6mol L-1
(5)在300时,如果向该容器中加入CO20.8 mol·L-1、H21.0 mol·L-1、CH4 2.8 mol·L-1、H2O 2.0mol·L-1,则该可逆反应初始速率v正_____v逆 (填“>” 或“<”)。
(6)若已知200℃时该反应的平衡常数K=64.8 则该反应的△H_________0(填“>”或“<”)。
Ⅲ.某高校的研究人员研究出一种方法,可实现水泥生产时CO2零排放,其基本原理如图所示
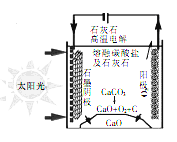
(7)上述电解反应在温度小于900℃时进行,碳酸钙先分解为CaO和CO2,电解质为熔融合碳酸钙,阴极的电极反应式为3CO2+4e- =C+2CO32-,则阳极的电极反应式为______________。