题目内容
【题目】NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
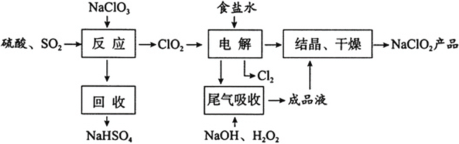
回答下列问题:
(1)NaClO2中Cl的化合价为________。
(2)写出“反应”步骤中生成ClO2的化学方程式____________________。
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去杂质Ca2+和SO42-,要加入的除杂试剂顺序为_________、________。“电解”中阴极反应的主要产物是____________。
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO2。此吸收反应中,氧化剂与还原剂的物质的量之比为________,该反应中氧化产物是________。
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。NaClO2的有效氯含量为________。(计算结果保留两位小数)
【答案】+32NaClO3+SO2+H2SO4== 2ClO2+2NaHSO4BaCl2溶液Na2CO3溶液NaClO22∶1O21.57g
【解析】
本题发生以下反应:NaClO3和SO2在H2SO4酸化条件下生成ClO2,此反应的化学方程式为:2NaClO3+SO2+H2SO4== 2ClO2+2NaHSO4;“电解”中阴极反应的主要产物是NaClO2;
“尾气吸收”反应为2NaOH+H2O2+2ClO2=2NaClO2+O2↑+2H2O ,以此分析解答。
(1)在NaClO2中Na为+1价,O为-2价,根据正负化合价的代数和为0,可得Cl的化合价为+3。
因此,本题正确答案是:+3;
(2)NaClO3和SO2在H2SO4酸化条件下生成ClO2,其中NaClO2是氧化剂,还原产物为NaCl,回收产物为NaHSO4,说明生成硫酸氢钠,且产生ClO2,根据电子守恒可知,此反应的化学方程式为:2NaClO3+SO2+H2SO4== 2ClO2+2NaHSO4,
因此,本题正确答案是:2NaClO3+SO2+H2SO4== 2ClO2+2NaHSO4;
(3)食盐溶液中混有Ca2+和SO42-,可以利用过量BaCl2溶液除去SO42-;利用过量Na2CO3溶液除去Ca2+及过量的Ba2+;由图可知“电解”中阴极反应的主要产物是NaClO2,
因此,本题正确答案是:BaCl2溶液;Na2CO3溶液;NaClO2;
(4)“尾气吸收”反应2NaOH+H2O2+2ClO2=2NaClO2+O2↑+2H2O中ClO2为氧化剂,还原产物为NaClO2,化合价从+4价降为+3价,H2O2为还原剂,氧化产物为O2,每摩尔H2O2得到2mol电子,依据电子守恒可知氧化剂和还原剂的物质的量之比为2:1,
因此,本题正确答案是:2:1;O2;
(5)1g NaClO2的物质的量![]() =
=![]() mol,依据电子转移数目相等,NaClO2~Cl-~4e-,Cl2~2Cl-~2e-,可知氯气的物质的量为
mol,依据电子转移数目相等,NaClO2~Cl-~4e-,Cl2~2Cl-~2e-,可知氯气的物质的量为![]() mol
mol ![]() =
=![]() mol,则氯气的质量为
mol,则氯气的质量为![]() mol ×71g/mol=1.57g,
mol ×71g/mol=1.57g,
因此,本题正确答案是:1.57g。

 考前必练系列答案
考前必练系列答案【题目】化学反应原理在工业生产中具有十分重要的意义。
(1)工业生产可以用NH3(g)与CO2(g)经两步反应生成尿素,两步反应的能量变化示意图如下:

则NH3(g)与CO2(g)反应生成尿素的热化学方程式为___________________________。
(2)已知反应Fe(s)+CO2(g) ![]() FeO(s)+CO(g) ΔH=a kJ·mol-1。测得在不同温度下,该反应的平衡常数K随温度的变化如下:
FeO(s)+CO(g) ΔH=a kJ·mol-1。测得在不同温度下,该反应的平衡常数K随温度的变化如下:
温度(℃) | 500 | 700 | 900 |
K | 1.00 | 1.47 | 2.40 |
①该反应的化学平衡常数K的表达式为____________,a________0(填“>”、“<”或“=”)。在500 ℃ 2 L密闭容器中进行反应,Fe和CO2的起始量均为4 mol,则5 min后达到平衡时CO2的转化率为________,生成CO的平均速率v(CO)为_______________。
②700 ℃反应达到平衡后,要使反应速率增大且平衡向右移动, 可采取的措施有 ___________。
(3)利用CO与H2可直接合成甲醇,下图是由“甲醇-空气”形成的绿色燃料电池的工作原理示意图,写出以石墨为电极的电池工作时负极的电极反应式_____________________,利用该电池电解1L 0.5mol/L的CuSO4溶液,当消耗560mLO2(标准状况下)时,电解后溶液的pH=_________(溶液电解前后体积的变化忽略不计)。


