题目内容
【题目】某班学生用0.1 mol·L-1盐酸和0.1 mol·L-1NaOH溶液反应测定酸碱滴定曲线,甲、乙、丙三组同学锥形瓶中的溶液所取体积均为20.00mL,且所用的试剂完全相同,根据实验所得的数据绘制的曲线分别如图中a、b、c所示,下列说法错误的是
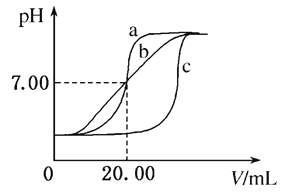
A.乙组同学操作上的不足是在滴定终点附近测试和记录pH的间隔太大
B.甲组同学滴定时选用的滴定管为酸式滴定管
C.乙和丙两组同学的操作均存在不足或失误
D.丙组同学可能是用待测液润洗了锥形瓶
【答案】B
【解析】
试题分析:A、pH=7附近溶液pH记录时间间隔过大体积变化大,误差大,A正确;B、图像分析,随加入溶液反应,溶液pH增大,说明是碱滴定酸,滴定是碱式滴定管,B错误;C、乙丙实验图像分析不正确,酸碱反应等浓度,等体积恰好反应,溶液呈中性,b曲线变化消耗溶液体积变化大,误差大,c曲线达到恰好反应消耗碱溶液大于20ml,乙和丙两组同学的操作上都存在着失误,乙组同学操作上的不足之处是在滴定终点附近测试和记录pH的间隔太大,C正确;D、图像分析丙曲线达到pH=7消耗碱溶液体积大于20ml,可能是待测夜润洗锥形瓶造成消耗碱溶液体积增多,D正确;答案选B。

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案
相关题目
【题目】甲、乙、丙、丁四位同学分别进行实验,测定四份不同澄清溶液的成分,记录如下
表,其中记录合理的是
甲 | K2SO4、BaCl2、NH4NO3 |
乙 | NaCl、Ca(OH)2、K2CO3 |
丙 | HCl、Na2SO3、NaCl |
丁 | K2SO4、NaNO3、KCl |
A.甲 B.乙 C.丙 D.丁