ĢāÄæÄŚČŻ
(10 ·Ö)ÓƵŖ»Æ¹č£ØSi3N4£©ĢÕ“É“śĢę½šŹōÖĘŌģ·¢¶Æ»śµÄÄĶČČ²æ¼ž£¬Äܓ󷳶ČĢįøß·¢¶Æ»śµÄČČŠ§ĀŹ”£¹¤ŅµÉĻÓĆ»ÆѧĘųĻą³Į»ż·ØÖʱøµŖ»Æ¹č£¬Ęä·“Ó¦ČēĻĀ£ŗ
3SiCl4(g) + 2N2(g) + 6H2(g)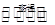 Si3N4(s) + 12HCl(g) ”÷H<0
Si3N4(s) + 12HCl(g) ”÷H<0
£Ø1£©ŌŚŅ»¶ØĪĀ¶ČĻĀ½ųŠŠÉĻŹö·“Ó¦£¬Čō·“ӦȯĘ÷µÄČŻ»żĪŖ2L£¬3minŗó“ļµ½Ę½ŗā£¬²āµĆ¹ĢĢåµÄÖŹĮæŌö¼ÓĮĖ1.40g£¬ŌņSiCl4µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ £»øĆ·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½ĪŖ ”£
£Ø2£©ÉĻŹö·“Ó¦“ļµ½Ę½ŗāŗó£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
a£®ĘäĖūĢõ¼ž²»±ä£¬ĪĀ¶ČÉżøߣ¬Ę½ŗā³£ŹżK¼õŠ”
b£®ĘäĖūĢõ¼ž²»±ä£¬Ń¹ĒæŌö“ó£¬Ę½ŗāĻņÕż·“Ó¦·½ĻņŅʶÆ
c£®ĘäĖūĢõ¼ž²»±ä£¬Ōö“óSiCl4ĪļÖŹµÄĮæ£¬Ę½ŗāĻņÕż·“Ó¦·½ĻņŅʶÆ
d£®ĘäĖūĢõ¼ž²»±ä£¬Ōö“óSi3N4ĪļÖŹµÄĮæ£¬Ę½ŗāĻņÄę·“Ó¦·½ĻņŅʶÆ
£Ø3£©Ņ»¶ØĢõ¼žĻĀ£¬ŌŚĆܱÕŗćČŻµÄČŻĘ÷ÖŠ£¬ÄܱķŹ¾ÉĻŹö·“Ó¦“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄŹĒ
a£®vÄę£ØN2£©=3vÕż£ØH2£© b£®vÕż£ØHCl£©=4vÄę£ØSiCl4£©
c£®»ģŗĻĘųĢåĆܶȱ£³Ö²»±ä d£®c(N2):c(H2):c(HCl)=1:3:6
£Ø4£©ČōĘ½ŗāŹ±H2ŗĶHClµÄĪļÖŹµÄĮæÖ®±ČĪŖm/n£¬±£³ÖĘäĖūĢõ¼ž²»±ä£¬½µµĶĪĀ¶Čŗó“ļµ½ŠĀµĀĘ½ŗāŹ±£¬H2ŗĶHClµÄĪļÖŹµÄĮæÖ®±Č m/n£ØĢī”°>”±”°=”±»ņ”°<”±£©
3SiCl4(g) + 2N2(g) + 6H2(g)
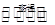 Si3N4(s) + 12HCl(g) ”÷H<0
Si3N4(s) + 12HCl(g) ”÷H<0£Ø1£©ŌŚŅ»¶ØĪĀ¶ČĻĀ½ųŠŠÉĻŹö·“Ó¦£¬Čō·“ӦȯĘ÷µÄČŻ»żĪŖ2L£¬3minŗó“ļµ½Ę½ŗā£¬²āµĆ¹ĢĢåµÄÖŹĮæŌö¼ÓĮĖ1.40g£¬ŌņSiCl4µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ £»øĆ·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½ĪŖ ”£
£Ø2£©ÉĻŹö·“Ó¦“ļµ½Ę½ŗāŗó£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
a£®ĘäĖūĢõ¼ž²»±ä£¬ĪĀ¶ČÉżøߣ¬Ę½ŗā³£ŹżK¼õŠ”
b£®ĘäĖūĢõ¼ž²»±ä£¬Ń¹ĒæŌö“ó£¬Ę½ŗāĻņÕż·“Ó¦·½ĻņŅʶÆ
c£®ĘäĖūĢõ¼ž²»±ä£¬Ōö“óSiCl4ĪļÖŹµÄĮæ£¬Ę½ŗāĻņÕż·“Ó¦·½ĻņŅʶÆ
d£®ĘäĖūĢõ¼ž²»±ä£¬Ōö“óSi3N4ĪļÖŹµÄĮæ£¬Ę½ŗāĻņÄę·“Ó¦·½ĻņŅʶÆ
£Ø3£©Ņ»¶ØĢõ¼žĻĀ£¬ŌŚĆܱÕŗćČŻµÄČŻĘ÷ÖŠ£¬ÄܱķŹ¾ÉĻŹö·“Ó¦“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄŹĒ
a£®vÄę£ØN2£©=3vÕż£ØH2£© b£®vÕż£ØHCl£©=4vÄę£ØSiCl4£©
c£®»ģŗĻĘųĢåĆܶȱ£³Ö²»±ä d£®c(N2):c(H2):c(HCl)=1:3:6
£Ø4£©ČōĘ½ŗāŹ±H2ŗĶHClµÄĪļÖŹµÄĮæÖ®±ČĪŖm/n£¬±£³ÖĘäĖūĢõ¼ž²»±ä£¬½µµĶĪĀ¶Čŗó“ļµ½ŠĀµĀĘ½ŗāŹ±£¬H2ŗĶHClµÄĪļÖŹµÄĮæÖ®±Č m/n£ØĢī”°>”±”°=”±»ņ”°<”±£©
(10 ·Ö)
£Ø1£©0.005mol”¤L-1”¤min-1£Ø2·Ö£© K=c12(HCl)/c6(H2)”¤c2(N2)”¤c3(SiCl4) £Ø2·Ö£©
£Ø2£©ac £Ø2·Ö£© £Ø3£©bc £Ø2·Ö£© £Ø4£©< £Ø2·Ö£©
£Ø1£©0.005mol”¤L-1”¤min-1£Ø2·Ö£© K=c12(HCl)/c6(H2)”¤c2(N2)”¤c3(SiCl4) £Ø2·Ö£©
£Ø2£©ac £Ø2·Ö£© £Ø3£©bc £Ø2·Ö£© £Ø4£©< £Ø2·Ö£©
ŹŌĢā·ÖĪö£ŗ
£Ø1£©3SiCl4(g) + 2N2(g) + 6H2(g)
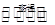 Si3N4(s) + 12HCl(g)
Si3N4(s) + 12HCl(g)3mol 140g
n 1.40g
3mol*1.40g=140g*n
½āµĆn=0.03mol
”÷c(SiCl4)= =0.03mol/2L=0.015mol/L”£
V(SiCl4)= ”÷c(SiCl4)/t=0.015(mol/L)/3min=0.005mol”¤L-1”¤min-1”£
»ÆŃ§Ę½ŗā³£ŹģµČÓŚ·“Ó¦ĪļµÄÅضČĆŻÖ®»ż³żŅŌÉś³ÉĪļµÄÅضČĆŻÖ®»żµÄÖµ£¬¼“
K= c12(HCl)/c6(H2)”¤c2(N2)”¤c3(SiCl4)”£
£Ø2£©b.Ōö“óŃ¹Ēæ£¬Ę½ŗāĻņĢå»ż¼õÉŁµÄ·½ĻņŅĘ¶Æ£¬¼“Ę½ŗāÄęĻņŅĘ¶Æ£¬¹Ź“ķ£»
d. Si3N4ŹĒ¹ĢĢ壬øıäĘäµÄĮæ£¬Ę½ŗā²»ŅĘ¶Æ£¬¹Ź“ķ£»
¹ŹŃ”ac”£
£Ø3£©a£®Ó¦ĪŖ3vÄę£ØN2£©=vÕż£ØH2£©£¬¹Ź“ķ£»d£®ÅØ¶ČµÄ±ČÖµ²»ÄÜÅŠ¶ØŹĒ·ńĘ½ŗāדĢ¬£¬¹Ź“ķ”£¹ŹŃ”bc”£
£Ø4£©½µµĶĪĀ¶Č£¬Ę½ŗāĻņ·ÅČČ·½ĻņŅĘ¶Æ£¬¼“ÕżĻņŅĘ¶Æ£¬¹ŹH2ŗĶHClµÄĪļÖŹµÄĮæÖ®±Č< m/n”£
µćĘĄ£ŗ±¾Ģāæ¼²é½ĻĪŖ×ŪŗĻ£¬Éę¼°·“Ó¦ĖŁĀŹ”¢Ę½ŗā³£Źż”¢Ę½ŗāŅʶÆŅŌ¼°µē»ÆѧµČÖŖŹ¶£¬ĢāÄæÄŃ¶Č²»“ó£¬×¢Ņā°ŃĪÕÓ°ĻģĘ½ŗāŅĘ¶ÆµÄŅņĖŲŅŌ¼°Ę½ŗāŅĘ¶Æ·½ĻņµÄÅŠ¶Ļ”£

Į·Ļ°²įĻµĮŠ“š°ø
 Ļ°Ģā¾«Ń”ĻµĮŠ“š°ø
Ļ°Ģā¾«Ń”ĻµĮŠ“š°ø
Ļą¹ŲĢāÄæ
 2NO2(g)£¬Õż·“Ó¦·ÅČČ”£²āµĆn(NO)Ėꏱ¼äµÄ±ä»ÆČēĻĀ±ķ£¬Ēė»Ų“š£ŗ
2NO2(g)£¬Õż·“Ó¦·ÅČČ”£²āµĆn(NO)Ėꏱ¼äµÄ±ä»ÆČēĻĀ±ķ£¬Ēė»Ų“š£ŗ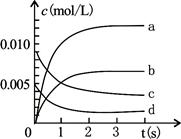
 2CO(g)·“Ó¦ÖŠæÉŹ¹·“Ó¦ĖŁĀŹŌö“óµÄ“ėŹ©ŹĒ””( )
2CO(g)·“Ó¦ÖŠæÉŹ¹·“Ó¦ĖŁĀŹŌö“óµÄ“ėŹ©ŹĒ””( )