题目内容
【题目】用化学用语解释相关现象正确的是( )
A.BaSO4的水溶液导电性极弱:BaSO4![]() Ba2++SO42-
Ba2++SO42-
B.KHSO4在熔融状态下可导电:KHSO4=K++H++SO42-
C.常温下,0.1mol/L的HF溶液的pH>1:HF+H2O![]() H3O++F-
H3O++F-
D.向KI-淀粉溶液中滴加稀硫酸,溶液变蓝色:4I-+O2+2H2O=2I2+4OH-
【答案】C
【解析】
试题分析:A.BaSO4的水溶液导电性极弱应该用其溶解度极小解释,故A错误;B.KHSO4在熔融状态下可导电,是因为熔融状态下能发生电离:KHSO4 = K++HSO4-,故B错误;C.常温下,0.1 mol/L的HF 溶液的pH>1,是因为HF是弱电解质,存在电离平衡:HF+H2O![]() H3O++F-,故C正确;D.向KI-淀粉溶液中滴加稀硫酸,溶液变蓝色,说明发生反应: 4I-+O2+4H+=2I2+2H2O,故D错误。故选C。
H3O++F-,故C正确;D.向KI-淀粉溶液中滴加稀硫酸,溶液变蓝色,说明发生反应: 4I-+O2+4H+=2I2+2H2O,故D错误。故选C。

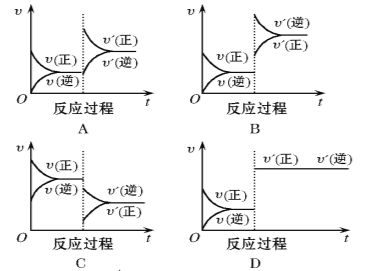
【题目】T℃时,将A和B各0.32 mol充入恒容密闭容器中,发生反应:A(g)+B(g)![]() 2C(g) △H=-a kJ·mol-1 (a>0),反应过程中测定的数据如下表,下列说法正确的是( )
2C(g) △H=-a kJ·mol-1 (a>0),反应过程中测定的数据如下表,下列说法正确的是( )
t/min | 0 | 2 | 4 | 7 | 9 |
n(B)/mol | 0.32 | 0.24 | 0.22 | 0.20 | 0.20 |
A.若起始时向容器中充入0.64 mol C,则达平衡时吸收的热量为0.12a kJ
B.恒温, 如果压缩容器体积,B的浓度和体积分数均不变
C.若起始时向容器中充入 0.64 mol A 和 0.64 mol B, 则达平衡时 n(C)<0.40 mol
D.恒温、恒容,向平衡体系中再充入0.32 mol A,再次平衡时,B的转化率增大
【题目】X、Y、Z、W、R是元素周期表前四周期中的常见元素,其相关信息如下表:
元素 | 相关信息 |
X | 组成蛋白质的基础元素,其最高正化合价与最低负化合价的代数和为2 |
Y | 地壳中含量最高的元素 |
Z | 存在质量数为23,中子数为12的核素 |
W | 生活中大量使用其合金制品,工业上可用电解熔融氧化物的方法制备其单质 |
R | 有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色 |
(1)R在元素周期表中的位置为______;X、Z、W三种元素的原子半径从大到小的顺序是________(用元素符号表示)。
(2)X与氢两元素按原子数目比1∶3和2∶4构成分子A和B,A的催化氧化方程式为_______;B的结构式为_______;化合物Z2Y中存在的化学键类型为________。
(3)W溶于Z的最高价氧化物的水化物的离子方程式_______________。
(4)用RCl3溶液腐蚀铜线路板的离子方程式为______。检验溶液中R3+常用的试剂是________,可以观察到的现象是________________。