题目内容
下列有关分子中指定原子的杂化类型正确的是( )
| A、CH4分子中C原子:sp |
| B、BF3中B原子:sp3 |
| C、C2H2中C原子:sp |
| D、SiO2中Si原子:sp2 |
考点:原子轨道杂化方式及杂化类型判断
专题:化学键与晶体结构
分析:根据中心原子的价层电子对数判断,烃中碳原子的杂化类型可以根据共价键数判断.
解答:
解:A、CH4分子中C原子形成4个C-H键,即含有4个σ电子对,所以是sp3杂化,故A错误;
B、BF3中B原子价层电子对数为3+
(3-3×1)=3,是sp2杂化,故B错误;
C、C2H2中C原子形成一个C≡C和2个C-H,含有2个σ电子对,所以是sp杂化,故C正确;
D、SiO2中Si原子与O原子形成4个共价键,即含有4个σ电子对,所以是sp3杂化,故D错误;
故选C.
B、BF3中B原子价层电子对数为3+
| 1 |
| 2 |
C、C2H2中C原子形成一个C≡C和2个C-H,含有2个σ电子对,所以是sp杂化,故C正确;
D、SiO2中Si原子与O原子形成4个共价键,即含有4个σ电子对,所以是sp3杂化,故D错误;
故选C.
点评:本题考查了原子的杂化类型的判断,注意根据中心原子的价层电子对数分析,题目难度不大.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
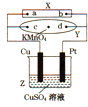 如图中X为电源,Y为浸透饱和硫酸钠溶液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向d端扩散,下列判断正确的是( )
如图中X为电源,Y为浸透饱和硫酸钠溶液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向d端扩散,下列判断正确的是( )| A、c电极的电极反应式为:2H++2e-=H2↑ |
| B、Cu电极质量减小,Pt电极质量增大 |
| C、Z中溶液的pH先减小,后增大 |
| D、a为电源正极,b为电源负极 |
下列数量的各物质所含原子个数由大到小顺序排列的是( )
①0.5mol氨气 ②4g氦气 ③4℃时9mL水 ④0.2mol磷酸钠.
①0.5mol氨气 ②4g氦气 ③4℃时9mL水 ④0.2mol磷酸钠.
| A、④③②① | B、①④③② |
| C、②③④① | D、①④②③ |
化学与科学、技术、社会、环境密切相关.下列有关说法正确的是( )
| A、合金材料中可能含有非金属元素 |
| B、酒精有消毒杀菌作用,医用酒精浓度越大杀菌效果越好 |
| C、地沟油含有有害物质,不能进行加工制生物柴油 |
| D、目前我市的汽油标准已由“国Ⅲ”提到“国Ⅳ”,这意味着汽车不再排放氮的氧化物 |
下列离子方程式中,不正确的是( )
| A、偏铝酸钠溶液中通入适量CO2:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- |
| B、向FeCl3溶液中滴加几滴KSCN溶液:Fe3++SCN-═[Fe(SCN)]2+ |
| C、NaHCO3与足量石灰水反应:2HCO3-+Ca2++2OH-═2H2O+CaCO3↓+CO32- |
| D、偏铝酸钠溶液中加过量盐酸:AlO2-+4H+═Al3++2H2O |
下列化合物中,既不能与NaOH溶液发生反应,又不能与溴的CCl4溶液发生反应,也不能使酸性KMnO4溶液褪色的是( )
| A、丙烷 | B、乙醇 | C、乙酸 | D、丙烯 |
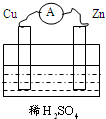 如图将Cu、Zn两种金属片插入稀H2SO4中,构成铜锌原电池,下列关于铜锌原电池的叙述正确的是( )
如图将Cu、Zn两种金属片插入稀H2SO4中,构成铜锌原电池,下列关于铜锌原电池的叙述正确的是( )| A、溶液中的H+向负极移动 |
| B、Zn片作负极,发生还原反应 |
| C、溶液的PH值将增大 |
| D、电子从Cu流出经导线流向Zn |
下列各组物质互为同系物的是( )
| A、金刚石和石墨 |
| B、正丁烷和异丁烷 |
| C、甲烷和乙烷 |
| D、白磷和红磷 |
化学与科技、社会、生产密切结合,下列有关说法正确的是( )
| A、“纯净水”清洁、纯净,长期饮用有益健康 |
| B、维生素C不宜与含硫酸亚铁的补血剂同服 |
| C、在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 |
| D、味觉上具有酸味的食物即酸性食物,长期食用会导致血液偏酸性,引起缺钙 |