题目内容
【题目】在一定条件下,N2O分解的部分实验数据如下:
反应时间/min | 0 | 10 | 20 | 30 | 40 | 50 |
c(N2O)/mol·L-1 | 0.100 | 0.090 | 0.080 | 0.070 | 0.060 | 0.050 |
反应时间/min | 60 | 70 | 80 | 90 | 100 | |
c(N2O)/mol·L-1 | 0.040 | 0.030 | 0.020 | 0.010 | 0.000 |
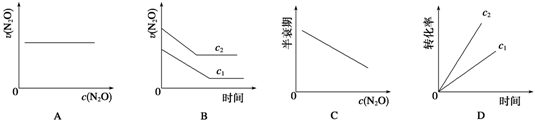
下图能正确表示该反应有关物理量变化规律的是 ( )
(注:图中半衰期指任一浓度N2O消耗一半时所需的相应时间,c1、c2均表示N2O初始浓度且c1<c2)
【答案】A
【解析】
试题分析:A.由表可知,每隔10min,c(N2O)的变化量相等,故单位时间内c(N2O)的变化量是定值,即N2O的分解速率是定值,A正确;B.由表可知,每隔10min,c(N2O)的变化量相等,故单位时间内c(N2O)的变化与N2O的起始浓度无关,最终N2O完全分解,B错误;C.0-50min,c(N2O)由0.1变为0.05,故0.1molL-1N2O的半衰期为50min,20-60min,c(N2O)由0.08变为0.04,故0.08molL-1N2O的半衰期为40min,故随着浓度的减小,半衰期也在减小,C错误;D.由表可知,每隔10min,c(N2O)的变化量相等,故N2O的起始浓度越小,单位时间内的转化率越大,最终N2O完全分解,D错误,答案选A。

【题目】下表列出9种元素在周期表中的位置,请按要求回答问题。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
4 | ⑨ |
(1)⑦的简单离子的结构示意图是______。表中标注的元素的最高价氧化物对应的水化物中碱性最强的碱是_____(填写化学式)。③、④、⑨三种元素按原子半径由大到小的顺序排列为 ______ (用元素符号表示)。
(2)元素②的气态氢化物的电子式是_______。由3个元素②的原子组成带一个单位负电荷的阴离子中含有_______个电子。写出该元素氢化物与其最高价氧化对应水化物反应的离子方程
式_____________。
(3)⑦、⑧两元素简单离子还原性强弱为______(填离子符号)。
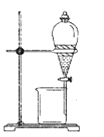
(4)某研究性学习小组设计了一组实验验证元周期律。
Ⅰ:甲同学在A、B两只烧杯里分别加入50mL水,再分别滴加几滴酚酞溶液,依次加入大小相近的③、⑨元素单质,观察现象。甲同学设计实验的目的是_____。写出元素⑨的单质与水反应的化学方程式为________。
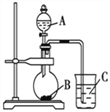
Ⅱ:乙同学设计如图装置以验证①、⑥、⑦元素的非金属性强弱。为了达到实验目的,仪器A、B、C分别选择的药品为A______、B______、C______;烧杯中发生反应的离子方程式为______________。