题目内容
与主族元素在元素周期表中所处的位置有关的是
A.相对原子质量 B.核内中子数
C.次外层电子数 D.电子层数和最外层电子数
【答案】
D
【解析】
试题分析:(长式)元素周期表中,把电子层数目相同的元素,按原子序数递增的顺序从左到右排成横行,再把不同横行中最外层电子数相同的元素,按电子层数递增的顺序由上而下排成纵行。故答案选D。
考点:元素周期表
点评:元素周期表是高考必考知识点,考生在备考中应掌握周期表的编排原则,并注意积累掌握短周期元素的结构与性质。

练习册系列答案
相关题目
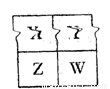
(14分)X、Y、Z、W、Q是原子序数依次增大的短周期主族元素,相关信息如下表:
| 元素 | 相关信息 |
| X | X原子核外最外层电子数是次外层的2倍 |
| Y | Y的气态氢化物的水溶液显弱碱性 |
| Z | Z是地壳中含量最多的金属元素 |
| W | 常温常压下,W的单质是淡黄色固体 |
| Q | …… |
 (1)元素Q在元素周期表中的位置______________________________.
(1)元素Q在元素周期表中的位置______________________________.(2)Y的最简单气态氢化物甲的水溶液可与H2O2发生反应,其产物不污染环境,化学方程式为______________________________________.(用元素符号表示,下同)
(3)X和氢元素组成的化合物分子有6个原子,其结构式为 .
(4)已知:X(s)+O2(g) =XO2(g) △H = -393.5kJ·mol-1
2X(s)+O2(g) ="2XO(g) " △H = -221.0kJ·mol-1
则XO的燃烧热的热化学方程式__________________________________________________.
(5)元素Y与氢元素形成的五核阳离子乙,向含乙和Z的阳离子的混合溶液中加入固体Na2O2,加入Na2O2的物质的量与产生沉淀有如图所示关系:
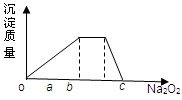
写出有关反应离子方程式:(每段只用一个离子方程式表示)
o—a段
a—b段 .
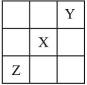
(22分)已知X、Y、Z三种短周期主族元素在元素周期表中的位置关系如图所示。
| Z | |
| Y | X |
(2)若X的单质是黄绿色气体,则X和Y的最高价氧化物对应的水化物的酸性强弱顺序为 (用化学式表示),和X同主族元素氢化物中熔沸点最高的是 (用化学式表示),原因是 ;X单质溶于水生成物之一具有漂白性,写出该物质结构式 。
(3)若X的单质与强酸、强碱溶液反应均能放出氢气,则元素X在周期表中的位置 写出X单质和烧碱溶液反应的离子方程式
探究X和Y两种元素金属性强弱的实验方法是 。
(4)若Y的氧化物是制造光导纤维的材料,则Y元素的名称是 ,
工业上利用单质Z和Y的氧化物高温下反应,生成一种具有空间立体网状结构的化合物,另一种生成物是有毒气体,写出反应化学方程式 。