��Ŀ����
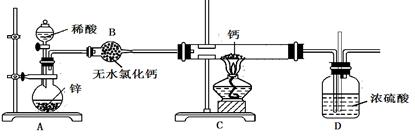
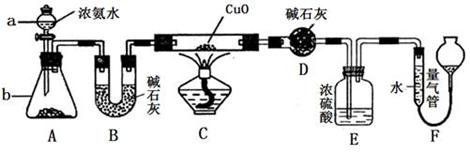
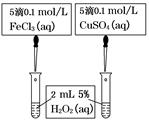
Ϊ̽����ҵ����������ͭ�Ͻ���ϵ������ã���ͬѧ��Ƶ�ʵ�鷽�����£�
��ش�
��1���̷��Ļ�ѧʽΪ ��
��2��д����Ӧ�ٵĻ�ѧ����ʽ ��
��Ӧ�����ɳ��������ӷ�Ӧ����ʽ ��
��3��Ϊ�˼����ҺD�к��еĽ������ӣ������ʵ�鷽��Ϊ���Լ���ѡ���� ��
��4��������B�еμ�ϡ����ʱ�����ַ�Ӧ���ʱ�һ������۷�ӦҪ�죬��ԭ���� ��
��5����������ɫ��ѧ���գ�������E�м���ϡ������Լ�Y�Ƶ������壬�Լ�YΪ��ɫҺ�壬��Ӧ�ܵ��ܻ�ѧ����ʽΪ ������������ɫ��ѧ���գ���ѡ�Լ�YΪ1mol/L�����ᣬ��ʹ3molCuȫ���ܽ�����Һ�к�ͭԪ�ص����ʽ�ΪCuSO4��������������� L��
��ʯ��
��1��FeSO4��7H2O
��2�� 2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2 �� ��
CO2 + 2H2O + AlO2- =Al(OH)3+ HCO3-
��3�����Թ�ȡ������ҺD������Һ�еμ�KSCN��Һ�����������ٵ�����ˮ�������Ѫ��ɫ����˵����Һ�д���Fe2+��
��4��ͭ������ϡ�����γ�ԭ���
��5��Cu + H2O2 +H2SO4 = CuSO4 + 2H2O �� 2
����

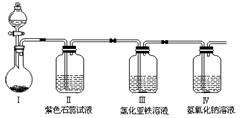
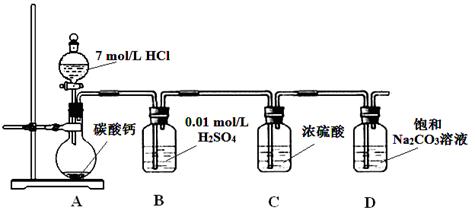
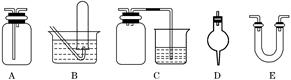
������ͼ��ʾװ����ȡ���������ռ���������
| A��п��ϡ���ᷴӦ������ |
| B��Ũ��ˮ���������ƹ��巴Ӧ�ư��� |
| C���������ƹ��������ᷴӦ�ƶ������� |
| D��ͭ��ϡ���ᷴӦ��һ������ |
�����仯�������ִ���ҵ�ϵ�Ӧ�ù㷺�������ڵ�ƣ�������ë��Ƥ���������������ϣ�����ӡˢ��������ý���ȡ����������ϸ��������彡���кܴ�Σ����
��ij�������Ƹ﹤ҵ������Cr��III�������������ù������£������ȡҺ�н���������Ҫ��Cr3+�������Fe3����Al3+��Ca2+��Mg2+����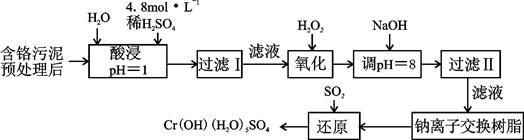
���������ӳ�����������������ʽ����ʱ��Һ��pH���±���
| ������ | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ |
| ��ʼ����ʱ��pH | 1.9 | 7.0 | ���� | ���� | 4.7 | ���� |
| ������ȫʱ��pH | 3.2 | 9.0 | 11.1 | 8 | 6.7 | 9 ����9�ܽ⣩ |
��1��ʵ������18.4 mol��L��1��Ũ��������250 mL 4.8 mol��L��1��������Һ�����õIJ����������ձ����������������ܣ�һ���ܾ�ȷ��ȡһ�����Һ����������⣬���� ��
��2�����ʱ��Ϊ����߽�ȡ�ʿɲ�ȡ�Ĵ�ʩ�� �����ٴ�һ�㣩��
��3��������Һ��pH=8��Ϊ�˳�ȥ ���ӡ������ӽ�����֬��ԭ��Ϊ��
Mn����nNaR��MRn��nNa�����������ĵ����������� ��
��4��Cr(OH)3����Һ�д������³����ܽ�ƽ�⣺Cr(OH)3(s)
 Cr3+(aq)+3OH��(aq)
Cr3+(aq)+3OH��(aq)�����£�Cr(OH)
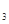 ���ܶȻ�Ksp= c(Cr3+)? c3(OH��)=10��32��Ҫʹc(Cr3+)����10��5mol/L����Һ��pHӦ���� ��
���ܶȻ�Ksp= c(Cr3+)? c3(OH��)=10��32��Ҫʹc(Cr3+)����10��5mol/L����Һ��pHӦ���� ����5����ԭ���̷������·�Ӧ������ƽ���� Na2Cr2O7�� SO2��
= Cr(OH) (H2O)5SO4�� Na2SO4��
��ҵ��ˮ�г�����һ������Cr2O72����CrO42�������ǻ�����༰��̬ϵͳ�����ܴ���������д�����
����һ�ִ�������Ϊ��ⷨ���÷���Fe���缫����⺬Cr2O72�������Է�ˮ�����ŵ����У�����������ҺpH���ߣ�����Cr(OH)3��������Fe���缫��ԭ��Ϊ
������������ҺpH���ߵ�ԭ���ǣ��õ缫��Ӧ���ͣ� ��
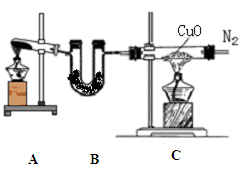
��11�֣�������㷺Ӧ������ҩ�ͻ�����ҵ��ijͬѧ�����üױ���������Ӧ�Ʊ������ᡣ��Ӧԭ����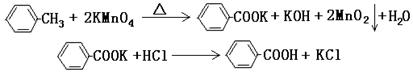
ʵ�鷽����һ�����ļױ���KMnO4��Һ��100�淴Ӧһ��ʱ���ֹͣ��Ӧ�����������̷����������ͻ���δ��Ӧ�ļױ���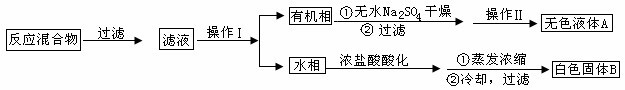
��֪����������Է���������122���۵�122.4�棬��25���95��ʱ�ܽ�ȷֱ�Ϊ0.3g��6.9g�����������л���һ�㶼�й̶��۵㡣
��1��������Ϊ ��������Ϊ ��
��2����ɫҺ��A�� �����Լ���A���Լ��� �������� ��
��3���ⶨ��ɫ����B���۵㣬��������115�濪ʼ�ۻ����ﵽ130��ʱ�����������ۡ���ͬѧ�Ʋ��ɫ����B�DZ�������KCl�Ļ�����������·��������ᴿ�ͼ��飬ʵ���������Ʋ���ȷ�����ڴ������ɱ������ݡ�
| ��� | ʵ�鷽�� | ʵ������ | ���� |
| �� | ����ɫ����B����ˮ�У����ȣ��ܽ⣬�� | �õ���ɫ�������ɫ��Һ | �������� |
| �� | ȡ������Һ���Թ��У� �� | ���ɰ�ɫ���� | ��Һ����Cl- |
| �� | �����ɫ���壬 �� | �� | ��ɫ�����DZ����� |
��4�����Ȳⶨ����ȡ1.220g��Ʒ�����100ml�״���Һ����ȡ25.00ml��Һ���ζ�������KOH�����ʵ���Ϊ2.40��10-3mol����Ʒ�б�������������Ϊ ��������λ��Ч���֣���