题目内容
二硫化亚铁是Li/FeS2电池的正极活性物质,可用水热法合成。FeSO4、Na2S2O3、S及H2O在200 ℃连续反应24 h,四种物质以等物质的量反应,再依次用CS2、H2O洗涤、干燥及晶化后得到。
(1)合成FeS2的离子方程式为_____________________________________。
(2)用水洗涤时,如何证明SO42—已除尽?________________________________________。
(3)已知1.20 g FeS2在O2中完全燃烧生成Fe2O3和SO2气体放出8.52 kJ热量,FeS2燃烧反应的热化学方程式为__________________________。
(4)取上述制得的正极材料1.120 0 g(假定只含FeS一种杂质),在足量的氧气流中充分加热,最后得0.800 0 g红棕色固体,试计算该正极材料中FeS2的质量分数(写出计算过程)。
(1)合成FeS2的离子方程式为_____________________________________。
(2)用水洗涤时,如何证明SO42—已除尽?________________________________________。
(3)已知1.20 g FeS2在O2中完全燃烧生成Fe2O3和SO2气体放出8.52 kJ热量,FeS2燃烧反应的热化学方程式为__________________________。
(4)取上述制得的正极材料1.120 0 g(假定只含FeS一种杂质),在足量的氧气流中充分加热,最后得0.800 0 g红棕色固体,试计算该正极材料中FeS2的质量分数(写出计算过程)。
(1)Fe2++S2O32—+S+H2O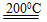 FeS2+2H++SO42—
FeS2+2H++SO42—
(2)取少许最后一次洗涤滤液,先用足量盐酸酸化,再向上述清液中滴加BaCl2溶液,若不出现白色浑浊,表示已洗涤干净
(3)4FeS2(s)+11O2(g)=2Fe2O3(s)+8SO2(g) ΔH=-3 408 kJ·mol-1
[或FeS2(s)+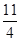 O2(g)=
O2(g)=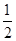 Fe2O3(s)+2SO2(g)] ΔH=-852 kJ·mol-1
Fe2O3(s)+2SO2(g)] ΔH=-852 kJ·mol-1
(4)解:120n(FeS2)+88n(FeS)=1.120 0
n(FeS2)+n(FeS)=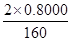
n(FeS2)=0.007 5 mol
w(FeS2)=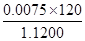 ≈0.803 6
≈0.803 6
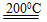 FeS2+2H++SO42—
FeS2+2H++SO42—(2)取少许最后一次洗涤滤液,先用足量盐酸酸化,再向上述清液中滴加BaCl2溶液,若不出现白色浑浊,表示已洗涤干净
(3)4FeS2(s)+11O2(g)=2Fe2O3(s)+8SO2(g) ΔH=-3 408 kJ·mol-1
[或FeS2(s)+
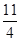 O2(g)=
O2(g)=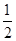 Fe2O3(s)+2SO2(g)] ΔH=-852 kJ·mol-1
Fe2O3(s)+2SO2(g)] ΔH=-852 kJ·mol-1(4)解:120n(FeS2)+88n(FeS)=1.120 0
n(FeS2)+n(FeS)=
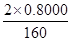
n(FeS2)=0.007 5 mol
w(FeS2)=
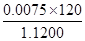 ≈0.803 6
≈0.803 6 (1)由题中信息可写出四种反应物,再由原子守恒和电荷守恒写出产物,Na2S2O3中一个S显+6价,一个S显-2价,其中-2的S与单质S发生归中反应,根据得失电子守恒配出反应。(2)检验SO42—,需要先用盐酸除去干扰离子,以防生成除BaSO4以外的钡盐沉淀。(3)0.01 mol FeS2完全燃烧放出8.52 kJ的热量。写热化学方程式要标注物质的状态,同时ΔH应与化学计量系数成比例。(4)由质量关系,列出120n(FeS2)+88n(FeS)=1.120 0,由铁原子守恒列出n(FeS2)+n(FeS)=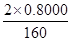 mol,联合解得FeS2的物质的量,进而求出其含量。
mol,联合解得FeS2的物质的量,进而求出其含量。
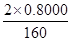 mol,联合解得FeS2的物质的量,进而求出其含量。
mol,联合解得FeS2的物质的量,进而求出其含量。
练习册系列答案
相关题目

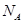
 2MO+4NO2↑+O2↑,加热29.6g M(NO3)2使其完全分解,在标准状况下收集11.2L的气体,那么M的摩尔质量是
2MO+4NO2↑+O2↑,加热29.6g M(NO3)2使其完全分解,在标准状况下收集11.2L的气体,那么M的摩尔质量是