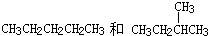题目内容
9.下列解释事实的离子方程式正确的是( )| A. | 铁和稀硝酸反应制得浅绿色溶液:Fe+4H++NO3-=Fe3++NO↑+2H2O | |
| B. | 实验室盛碱液的瓶子不用玻璃塞:SiO2+2OH-=SiO32-+H2O | |
| C. | 用稀盐酸和大理石反应制取CO2:CO32-+2H+=CO2↑+H2O | |
| D. | 向Ca(ClO)2溶液中通入过量CO2制取次氯酸:2ClO-+H2O+CO2=2HClO+CO32- |
分析 A.反应制得浅绿色溶液,说明生成的是亚铁离子,不是铁离子;
B.玻璃塞中含有二氧化硅,二氧化硅能够与氢氧根离子反应;
C.大理石的主要成分为碳酸钙,碳酸钙为难溶物,不能拆开;
D.二氧化碳过量,反应生成碳酸氢根离子.
解答 解:A.铁和稀硝酸反应制得浅绿色溶液,则反应生成了亚铁离子,正确的离子方程式为:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O,故A错误;
B.实验室盛碱液的瓶子不用玻璃塞,原因是玻璃塞中含有二氧化硅,二氧化硅能够与氢氧根离子反应,反应的离子方程式为:SiO2+2OH-=SiO32-+H2O,故B正确;
C.碳酸钙为难溶物,需要保留化学式,正确的离子方程式为:CaCO32-+2H+=CO2↑+H2O+Ca2+,故C错误;
D.Ca(ClO)2溶液中通入过量CO2制取次氯酸,反应生成次氯酸和碳酸氢根离子,正确的离子方程式为:ClO-+H2O+CO2=HClO+HCO3-,故D错误;
故选B.
点评 本题考查了离子方程式的书写判断,题目难度中等,明确离子方程式的书写原则为解答关键,注意掌握常见的需要保留化学式的物质,如难溶物、氧化物、弱电解质、气体等,试题培养了学生的灵活运用能力.

练习册系列答案
相关题目
20.下列制备和收集气体的实验装置合理的是( )
| A. |  用氯化铵和氢氧化钙制NH 3 | B. | 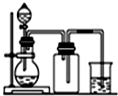 用铜片和稀硝酸制NO | ||
| C. | 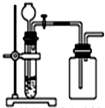 用锌粒和稀硫酸制H 2 | D. | 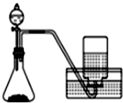 用双氧水和二氧化锰制O2 |
17.如表中关于物质分类的正确组合是( )
| 类别组合 | 酸性氧化物 | 碱性氧化物 | 酸 | 碱 | 盐 |
| A | NO2 | CuO | H2SO4 | NH3•H2O | Na2S |
| B | CO2 | Na2O | CH3COOH | NaOH | NaHCO3 |
| C | SO2 | Al2O3 | HCl | KOH | NaCl |
| D | SO3 | CaO | HNO3 | Na2CO3 | CaCO3 |
| A. | A | B. | B | C. | C | D. | D |
4.现有反应:4NH3+5O2═4NO+6H2O,反应速度分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,其关系正确的是( )
| A. | 4v(NH3)=5v(O2) | B. | 4v(NH3)=6v(H2O) | C. | 4v(O2)=5v(NO) | D. | 4v(NH3)=5v(NO) |
14.下列微粒中,不具有氧化性的是( )
| A. | Cl2 | B. | O | C. | H+ | D. | S2- |
1.在1000mL NaOH溶液中加入足量铝粉,反应完全后共收集到标准状况下的气体33.6L,该NaOH溶液的浓度为( )
| A. | 1.0 mol/L | B. | 2.0 mol/L | C. | 1.5 mol/L | D. | 3.0 mol/L |
 E.
E.