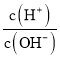��Ŀ����
����Ŀ����ͭ�Ͻ�㷺���ں��չ�ҵ������ͭ�Ͻ���и�����л��������Ʊ����뵼�籡Ĥ���ϣ�CuAlO2���Ĺ������£�
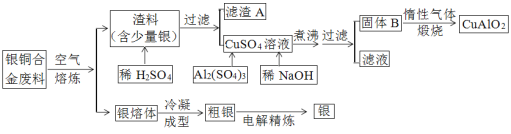
ע��Al(OH)3��Cu(OH)2�ֽ���¶ȷֱ�Ϊ450����80����
��1���ӿ����ϣ���������������ϡH2SO4�����ʵĴ�ʩ��_______��д��һ�֣���
��2������A��ϡHNO3��Ӧ�������������ڿ�����Ѹ�ٱ�Ϊ����ɫ��д������A������ϡHNO3��Ӧ�Ļ�ѧ����ʽΪ_______��
��3�����CuSO4�����Һ�Ĺ����У��õ�����B�������B�ijɷ�Ϊ_______�������ɹ���B�Ĺ����У������NaOH�ļ������ͷ�ֹ�μ�ʱNaOH�����ֲ����ɷ�ֹ����NaOH�����ֲ�����IJ�����_______����NaOH�����������������ķ�Ӧ�����ӷ���ʽΪ_______��
��4����֪���ڳ�����Cu(OH)2��Ksp=2��1020 mol3��L3��������0.02 mol��L1CuSO4��Һ���Ҫ����Cu(OH)2������Ӧ������Һ��pH��ʹ֮����_________��
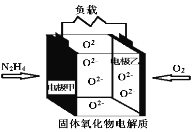
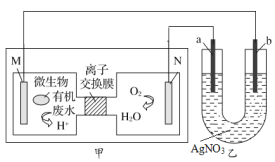
��5��ͼ�м�Ϊ���ォ�л���ˮ�Ļ�ѧ��ת��Ϊ���ܵ�һ��������ˮ����װ�ã����ø�װ�ý��е�⾫����ʱ������ӦΪ��װ�õ�_______������a������b��������b�缫��ӦʽΪ_______����N�缫����1.12 L����״���£�O2ʱ������װ�����������ܲ���_______ g����
���𰸡���������Ũ�Ȼ������¶Ȼ��������� 3Ag+4HNO3(ϡ) =3AgNO3+NO��+2H2O Al(OH)3��CuO ����������NaOH�������Ͻ��� Al(OH)3+OH=AlO2+2H2O �� Al(OH)3+OH===[Al(OH)4]- 5 a Ag++e=Ag 21.6
��������
Ag��Cu�Ͻ�����ڿ����������õ�Ag���壬Ag�����������͵õ���Ag����Ag��⾫���õ�Ag�������к�������Ag��CuO���������м���ϡ���ᣬ������ӦCuO+H2SO4=CuSO4+H2O�����˵õ�����AΪAg����Һ�к���CuSO4��Al(OH)3��Cu(OH)2��ʼ�ֽ���¶ȷֱ�Ϊ450���80�棬������ͭ��Һ�м�����������NaOH��Һ���õ�Al(OH)3��Cu(OH)2����й�����������ͭ�ֽ�����CuO��Ȼ����˵õ�����BΪAl(OH)3��CuO������B�ڶ��������Χ�����յõ�CuAlO2���Դ˽����⡣
(1)�ӿ����ϣ���������������ϡH2SO4���ʵĴ�ʩΪ���衢���Ϸ��顢�ʵ����¡��ʵ�����H2SO4��Ũ�ȵȣ�
(2)Ag��ϡ���ᷴ����Ӧ������AgNO3��NO����ѧ����ʽΪ3Ag+4HNO3(ϡ) =3AgNO3+NO��+2H2O��
(3)Al(OH)3��Cu(OH)2��ʼ�ֽ���¶ȷֱ�Ϊ450���80�棬������ͭ��Һ�м�����������NaOH��Һ���õ�Al(OH)3��Cu(OH)2����й�����������ͭ�ֽ�����CuO��Ȼ����˵õ�����BΪAl(OH)3��CuO��
NaOH�����ֲ�����˵��û�л�Ͼ��ȣ������ڿ���NaOH�ĵμ��ٶȣ������裻
��NaOH��������Al(OH)3�����ڹ�����NaOH�����ӷ���ʽΪAl(OH)3+OH=AlO2+2H2O��
(4) Cu(OH)2��Ksp=2��1020 mol3��L3��![]() ��0.02 mol��L1CuSO4��Һ��c(Cu2��)=0.02mol��L��1���������ݣ�
��0.02 mol��L1CuSO4��Һ��c(Cu2��)=0.02mol��L��1���������ݣ�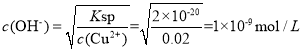 ��
��![]() ��
��![]() ����pHӦ�ô���5��
����pHӦ�ô���5��
(5)���ұ��ʱ������������������������������ԭ����У�ͨ��O2��һ��Ϊ��������֪NΪ������aΪ������bΪ������MΪ�����������ӦΪ��װ���е�a����
bΪ��������Һ�е�Ag���õ����ӣ��缫����ʽΪAg++e=Ag��
��N�缫����1.12 L����״���£�O2ʱ��O�Ļ��ϼ۴�0���͵���2�ۣ�����1.12 LO2����0.05mol��ת�Ƶĵ�����Ϊ0.05mol��2��2=0.2mol���ӣ���ͬһ����·�У�����ת�Ƶĵ�������ͬ����װ����b������Ag���ʣ����ݵ缫����ʽ��ת��0. 2mol���ӣ�����0.2molAg��������Ϊ0.2mol��108g��mol��1=21.6g��