题目内容
18.下列离子反应方程式正确的是( )| A. | 硫酸铝与氨水反应:Al3++3OH-═Al(OH)3↓ | |
| B. | 碳酸钙溶于醋酸:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| C. | 少量Ca(OH)2溶液与大量NaHCO3溶液:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| D. | 盐酸中滴入Na2CO3溶液:2H++CO32-═CO2↑+H2O |
分析 A.一水合氨为弱电解质,保留化学式;
B.醋酸为弱电解质,保留化学式;
C.反应生成碳酸钙、碳酸钠和水;
D.反应生成氯化钠、水和二氧化碳.
解答 解:A.硫酸铝与氨水反应,离子方程式:Al3++3NH3.H2O=Al(OH)3↓+3NH4+,故A错误;
B.碳酸钙溶于醋酸,离子方程式:CaCO3+2CH3COOH═Ca2++H2O+CO2↑+2CH3COO-,故B错误;
C.少量Ca(OH)2溶液与大量NaHCO3溶液,离子方程式:Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32-,故C错误;
D.盐酸中滴入Na2CO3溶液,离子方程式:2H++CO32-═CO2↑+H2O,故D正确;
故选:D.
点评 本题考查离子反应的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,注意化学式的拆分,题目难度不大.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
8.有一种有机化合物,其结构简式如下,下列有关它的性质叙述中,正确的是( )
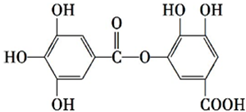

| A. | 有弱酸性,能与NaHCO3溶液反应 | |
| B. | 在一定条件下,1 mol该物质最多能与7 mol NaOH完全反应 | |
| C. | 在一定条件下,1 mol该物质可以和8 mol H2发生加成反应 | |
| D. | 能发生水解反应,水解后能生成两种物质 |
6.下列各组离子能在强酸性的溶液中大量共存,且溶液呈无色的是( )
| A. | K+、Na+、MnO4-、SO42- | B. | K+、Na+、CO32-、Cl- | ||
| C. | Mg2+、NH4+、Cl-、NO3- | D. | Ba2+、K+、OH-、SO42- |
13.下列反应中,熵变小于0的是( )
| A. | (NH4 )2CO3(s)═NH4HCO3(s)+NH3(g) | B. | 2N2O5(g)═4NO2(g)+O2(g) | ||
| C. | MgCO3(s)═MgO(s)+CO2(g) | D. | 2CO(g)═2C(s)+O2(g) |
8.下列关于金属腐蚀与防护的说法正确的是( )
| A. | 金属腐蚀就是金属失去电子被还原的过程 | |
| B. | 铝制品的耐腐蚀性强,说明铝的化学性质不活泼 | |
| C. | 将海水中钢铁闸门与电源的负极相连,可防止闸门被腐蚀 | |
| D. | 钢铁锈蚀时,铁失去电子成为Fe3+,而后生成Fe(OH)3,再部分脱水成为氧化铁的水合物 |

 )是比较简单的稠环芳香烃.请回答以下问题:
)是比较简单的稠环芳香烃.请回答以下问题: ;
;