题目内容
【题目】某离子化物MCl(s)在水中溶解并发生电离,该过程的微观示意图如图。已知NA为阿伏伽德罗常数的值。下列相关说法正确的是( )
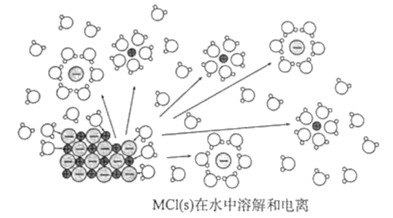
A.1molMCl中含有NA对共用电子对
B.MCl为弱电解质,在水中仅部分电离
C.M+和Cl-均与水分子中的氧原子结合形成水合离子
D.MCl在水作用下的溶解和电离过程是物理变化
【答案】D
【解析】
A. MCl为离子化合物,不存在共用电子对,A错误;
B. MCl为离子化合物,故MCl为强电解质,在水中完全电离,B错误;
C. M+与水分子中的氧原子结合形成水合离子、Cl-与水分子中的氢原子结合形成水合离子,C错误;
D. MCl在水作用下的溶解和电离过程中没有新物质生成,是物理变化,D正确;
答案选D。

练习册系列答案
相关题目
【题目】下图是物质间发生化学反应的颜色变化,下表选项物质对应正确的是
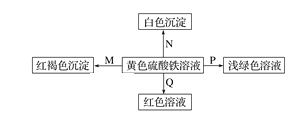
选项 | M | N | P | Q |
A | NH3·H2O | Ba(OH)2 | 铜 | KSCN |
B | Na | BaCl2 | FeO | KSCN |
C | NaOH | Ba(NO3)2 | 锌粉 | KSCN |
D | Na2O2 | MgCl2 | Fe | KSCN |
A.AB.BC.CD.D
【题目】在3种不同条件下,分别向容积为1L的恒容密闭容器中充入4molA和2molB,发生反应:2A(g)+B(g)![]() 2D(g) △H=QkJ/mol,相关条件和数据见表。下列说法正确的是( )
2D(g) △H=QkJ/mol,相关条件和数据见表。下列说法正确的是( )
实验编号 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
反应温度/℃ | 700 | 700 | 750 |
达平衡时间/min | 40 | 5 | 30 |
n(D)平衡/mol | 3 | 3 | 2 |
化学平衡常数 | K1 | K2 | K3 |
A.实验Ⅲ达平衡后,恒温下再向容器中通入2 molA和2 molD,平衡正向移动
B.升高温度能加快反应速率的原理是降低了活化能,使活化分子百分数提高
C.实验Ⅰ达平衡后容器内的压强是实验Ⅲ的0.9倍
D.K3<K2 =K1