题目内容
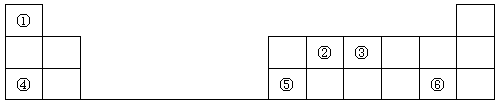
下列顺序表述正确的是( )
| A.酸性:H3PO4> HNO3> HClO4 | B.稳定性:H2O > HF > H2S |
| C.原子半径:Na > Mg > O | D.还原性:F-> Cl-> S2- |
C
同周期,由左到右,原子的得电子能力逐渐增强,则最高价氧化物对应水化物的酸性逐渐增强;同主族,由上到下,原子的得电子能力逐渐减弱,则最高价氧化物对应水化物的酸性逐渐增强减弱,且是最强的含氧酸,故酸性:HClO4 > HNO3> H3PO4 ;
同周期,由左到右,原子的得电子能力逐渐增强,则气态氢化物的稳定性逐渐增强;同主族,由上到下,原子的得电子能力逐渐减弱,则气态氢化物的稳定性逐渐减弱;故稳定性:HF> H2O > H2S;
同周期,由左到右,原子半径逐渐减小;同主族,由上到下,原子半径逐渐增大;故原子半径:Na > Mg >S >O,则C正确;
同周期,由左到右,原子的得电子能力逐渐增强,则单质的氧化性逐渐增强,其阴离子的还原性逐渐减弱;同主族,由上到下,原子的得电子能力逐渐减弱,则单质的氧化性逐渐减弱,其阴离子的还原性逐渐增强;故还原性:S2-> Cl-> F-;
同周期,由左到右,原子的得电子能力逐渐增强,则气态氢化物的稳定性逐渐增强;同主族,由上到下,原子的得电子能力逐渐减弱,则气态氢化物的稳定性逐渐减弱;故稳定性:HF> H2O > H2S;
同周期,由左到右,原子半径逐渐减小;同主族,由上到下,原子半径逐渐增大;故原子半径:Na > Mg >S >O,则C正确;
同周期,由左到右,原子的得电子能力逐渐增强,则单质的氧化性逐渐增强,其阴离子的还原性逐渐减弱;同主族,由上到下,原子的得电子能力逐渐减弱,则单质的氧化性逐渐减弱,其阴离子的还原性逐渐增强;故还原性:S2-> Cl-> F-;

练习册系列答案
相关题目